题目内容
(14分)X、Y、Z三种化合物均由短周期元素组成。已知三种化合物的水溶液的焰色反应均呈黄色,Y和Z均由三种元素组成。请根据题目的要求回答下列问题。
(1)固体化合物X为浅黄色粉末,该化合物中含有化学键为 (填序号)。
A.离子键 B.极性共价键 C.非极性共价键
(2)写出X与二氧化碳反应的化学方程式 。
(3)下表为Y和Z实验的部分内容
写出含0.1 mol Z的溶液与20 mL 5mol/L的盐酸反应的离子方程式:
实验③加热蒸发、灼烧得到的最终产物主要是 和 。
(4)写出Y与稀硫酸反应的离子方程式 。
(1)固体化合物X为浅黄色粉末,该化合物中含有化学键为 (填序号)。
A.离子键 B.极性共价键 C.非极性共价键
(2)写出X与二氧化碳反应的化学方程式 。
(3)下表为Y和Z实验的部分内容
| 序号 | 主要实验步骤及实验现象 |
| ① | 在Y的无色溶液中,加入稀硫酸,放置。产生浅黄色沉淀和无色有刺激性气味的气体。该气体可使品红溶液褪色。 |
| ② | 在Z的无色溶液中,滴加的盐酸,开始有白色沉淀,继续滴加盐酸,白色沉淀先增加后消失,然后加入过量的氨水又出现白色沉淀。 |
| ③ | 将实验②最终得到的混合物加热蒸发、灼烧,最终得到固体。 |
实验③加热蒸发、灼烧得到的最终产物主要是 和 。
(4)写出Y与稀硫酸反应的离子方程式 。
(1)AC;(2)2Na2O2 + 2CO2 = 2Na2CO3 + O2↑;
(3)AlO2—+ H+ + H2O = Al(OH)3↓;NaCl和Al2O3;
(4)S2O32—+2H+=S↓+SO2↑+H2O
(3)AlO2—+ H+ + H2O = Al(OH)3↓;NaCl和Al2O3;
(4)S2O32—+2H+=S↓+SO2↑+H2O
根据焰色反应可知均为钠盐,固体化合物X为过氧化钠,Y 为Na2S2O3,Z为NaAlO2 。2Na2O2 + 2CO2 = 2Na2CO3 + O2↑;AlO2—+ H+ + H2O = Al(OH)3↓;S2O32—+2H+=S↓+SO2↑+H2O。

练习册系列答案
相关题目

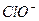 、
、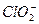 、
、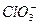 、
、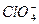 中Cl都是以sp3杂化轨道与O原子成键的,试推测下列微粒的立体结构
中Cl都是以sp3杂化轨道与O原子成键的,试推测下列微粒的立体结构 2HCl+2COCl2。为防止发生医疗事故,使用前可用于检验氯仿是否变质的试剂是(填序号) 。
2HCl+2COCl2。为防止发生医疗事故,使用前可用于检验氯仿是否变质的试剂是(填序号) 。