��Ŀ����
����Ŀ������������գ�
��1����ҵ������CO2��NH3��ϣ���һ�������·�Ӧ�ϳ����أ� 2NH3��g��+CO2��g�� ![]() CO��NH2��2��S��+H2O��g����H
CO��NH2��2��S��+H2O��g����H
���÷�Ӧ��һ���¡������ܱ������ڽ��У��жϷ�Ӧ�ﵽƽ��״̬�ı�־�� ��
a��CO2��H2O��g��Ũ����� b�������������ѹǿ���ٸı�
c��2v��NH3����=v��H2O���� d�������а�����Ũ�Ȳ��ٸı�
��2������п�ɹ㷺����ӡȾýȾ����ľ�ķ������� ZnSO4���ȷֽ�����и��������ʵ������¶ȱ仯��ϵ��ͼ1��ʾ�� 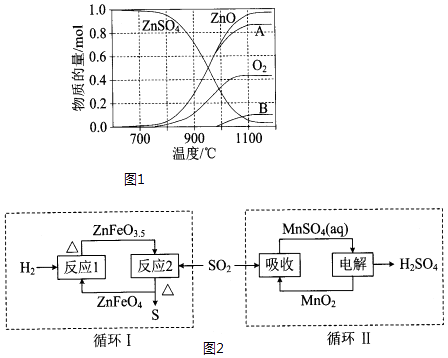
��д��700�桫980��ʱ������Ӧ�Ļ�ѧ����ʽ�� �� ����B�Ļ�ѧʽ�� �� ��A��B��Ϊ��������
������п�ֽ����ɵ�SO2��ͼ2�е�����ѭ���ɷֱ�õ�S��H2SO4 �� д��ѭ��I�з�Ӧ2�Ļ�ѧ����ʽ����ѭ��II���ö��Ե缫��⣬������Ӧʽ�� ��
���𰸡�
��1��bd
��2��2ZnSO4![]() 2ZnO+2SO2��+O2���� SO2��4ZnFeO3.5+SO2
2ZnO+2SO2��+O2���� SO2��4ZnFeO3.5+SO2![]() 4ZnFeO4+S�� Mn2+��2e��+2H2O=MnO2+4H+
4ZnFeO4+S�� Mn2+��2e��+2H2O=MnO2+4H+
���������⣺��1��a��CO2��H2O��g��Ũ����ȣ������Dz��䣬�ʴ���
b�������������ѹǿ���ٸı䣬˵����������ʵ������䣬��Ӧ��ƽ��״̬������ȷ��
c��2v��NH3����=v��H2O����������������Ӧ����δ����������Ĺ�ϵ���ʴ���
d�������а�����Ũ�Ȳ��ٸı䣬˵�����������ʵ������䣬��Ӧ��ƽ��״̬������ȷ��
��ѡ��bd����2����700�桫980��ʱ������Ӧʱ������ͼ֪������ZnO��������B������Ԫ���غ�֪��B�к���SԪ�أ���Ϊ��������ʧ���ӣ���SԪ��Ӧ�õõ��ӷ�����ԭ��Ӧ������BӦ����SO2�����ݷ�Ӧ��������P��Ӧ������д����ʽΪ2ZnSO4 ![]() 2ZnO+2SO2��+O2�������Դ��ǣ�2ZnSO4
2ZnO+2SO2��+O2�������Դ��ǣ�2ZnSO4 ![]() 2ZnO+2SO2��+O2����SO2��
2ZnO+2SO2��+O2����SO2��
��ZnFeO3.5��SO2�ڼ�������������ZnFeO4��S����Ӧ����ʽΪ4ZnFeO3.5+SO2 ![]() 4ZnFeO4+S��
4ZnFeO4+S��
���������ʱ�����ɶ������̺����ᣬ������ʧ���ӷ���������Ӧ���缫��ӦʽΪMn2+��2e��+2H2O=MnO2+4H+��
���Դ��ǣ�4ZnFeO3.5+SO2 ![]() 4ZnFeO4+S��Mn2+��2e��+2H2O=MnO2+4H+��
4ZnFeO4+S��Mn2+��2e��+2H2O=MnO2+4H+��
�����㾫����ͨ��������û�ѧƽ��״̬���жϣ�����״̬�жϣ���v(B��)=v(B��)��v(C��):v(D��)=x : y��c(C)��C%��n(C)%�Ȳ������A��B��C��DΪ���壬��m+n��x+y��ѹǿ�㶨����ϵ��ɫ�����λʱ����ij�����ڻ�ѧ���Ķ����������γ�������ϵƽ��ʽ���㶨��m+n �� x+y���ȼ����Խ����⣮

����Ŀ���������ȼҵ����Ҫ��Ʒ֮һ������ǿ�������������л����������з�Ӧ���ɶ����Ȼ��ij��ȤС����ʵ�����ж����·�Ӧ������̽�����ش��������⣺
�������Ȼ���(BCl3)���Ʊ�����֪����BCl3�ķе�Ϊ12.5 �����۵�Ϊ��107.3 ���� ��2B��6HCl ![]() 2BCl3����3H2����
2BCl3����3H2����

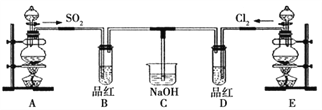
��1���������������Ӹ�װ�õĽӿڣ�˳��Ϊa��( )��( )��( )��( )��( )��( )��f��g��h��_________
��2��װ��D��������_____________��ʵ����������װ��C�����ܲ�����Σ����____________��
��3��BCl3��ˮ����ˮ��۲쵽�����İ��������������ᣬ�䷴Ӧ�Ļ�ѧ����ʽΪ��___________��
����SO2��Ư�۾���Һ�ķ�Ӧ
���� | ���� |
ȡ4g Ư�۾����壬����100mL ˮ����Ư�۾���Һ��pH | pH ��ֽ�ȱ�����ԼΪ12��������ɫ |
| 1.Һ���Ϸ����ְ����� 2.�Ժ��ֻ��ǣ���Һ��Ϊ����ɫ�� 3.�Ժ���������ɫ����������ɫ��ȥ |
��4��pH��ֽ��ɫ�ı仯˵��Ư�۾���Һ���е�������_____________________________��
��5������2����Һ��Ϊ����ɫ��ԭ���ǣ�����Һ���Ե���ǿ��Ư�۾�����Ч�ɷֺ�Cl- ������Ӧ���÷�Ӧ�����ӷ���ʽΪ________________________��
��6�������ӷ���ʽ��������3�л���ɫ��ȥ��ԭ��_______________________��