题目内容
6.已知可由乙烯合成高分子材料G.
F的质谱图中最大质荷比为86,其C、H、O的原子个数之比为2:3:1,F在酸性条件下水解可生成碳原子数相同的两种有机物D和E.请回答下列问题:
(1)B的分子式为C2H6O,F分子含氧官能团的名称为酯基.
(2)E的结构简式为CH3CHO,G的结构简式为
 .
.(3)反应①、⑥的反应类型均是加成反应.
(4)反应②的化学方程式为CH2BrCH2Br+2NaOH$→_{△}^{乙醇}$HC≡CH+2NaBr+2H2O.
(5)在F的同分异构体中,核磁共振氢谱有三个峰,三个峰的面积之比为1:1:1,任意写出其中一种满足上述条件的结构简式
 .
.
分析 F的质谱图中最大质荷比为86,其中C、H、O的原子个数之比为2:3:1,设分子式为(C2H3O)x,则43x=86,x=2,分子式为C4H4O2,由图给转化关系可知A为CH2BrCH2Br,C为HC≡CH,B为CH3CH2OH,D为CH3COOH,F为CH2=CHOOCCH3,E为CH3CHO,G为 ,结合对应的有机物的结构和性质以及题目要求解答该题.
,结合对应的有机物的结构和性质以及题目要求解答该题.
解答 解:F的质谱图中最大质荷比为86,其中C、H、O的原子个数之比为2:3:1,设分子式为(C2H3O)x,则43x=86,x=2,分子式为C4H4O2,由图给转化关系可知A为CH2BrCH2Br,C为HC≡CH,B为CH3CH2OH,D为CH3COOH,F为CH2=CHOOCCH3,E为CH3CHO,G为 ,
,
(1)B为CH3CH2OH,分子式为C2H6O,F为CH2=CHOOCHCH3,含有的官能团为酯基,故答案为:C2H6O;酯基;
(2)由以上分析可知E为CH3CHO,G为 ,故答案为:CH3CHO;
,故答案为:CH3CHO; ;
;
(3)反应①、⑥的反应类型均是加成反应,故答案为:加成反应;
(4)反应②为CH2BrCH2Br的消去反应,反应的方程式为CH2BrCH2Br+2NaOH$→_{△}^{乙醇}$HC≡CH+2NaBr+2H2O,
故答案为:CH2BrCH2Br+2NaOH$→_{△}^{乙醇}$HC≡CH+2NaBr+2H2O;
(5))F为CH2=CHOOCHCH3,对应的同分异构体中,核磁共振氢谱有三个峰,三个峰的面积之比为1:1:1,可能的结构有 ,
,
故答案为: .
.
点评 本体考查有机物的合成与推断,综合考查学生的分析能力、推断能力和综合运用化学知识的能力,为高考常见题型,难度较大,注意把握题给信息,该题的关键是记住常见官能团的结构、性质以及官能团之间的相互转化,然后结合题意灵活运用即可.

 以Al和NiO(OH)为电极,NaOH溶液为电解液组成一种新型电池,通过电解原理来降解酸性废水中的NO3-,下列说法错误的是( )
以Al和NiO(OH)为电极,NaOH溶液为电解液组成一种新型电池,通过电解原理来降解酸性废水中的NO3-,下列说法错误的是( )| A. | 该新型电池工作时,负极的电极反应式是Al+4OH--3e-═AlO2-+2H2O | |
| B. | 为增强溶液的导电性,I区水中可加入少量Na2SO4 | |
| C. | A为电源正极,H+从Ⅰ区移向Ⅱ区 | |
| D. | 阴极反应式为:2NO3-+6H2O+10e-═N2↑+12OH- |
| A. | B和C可能都是固体 | B. | B和C一定都是气体 | ||
| C. | 若C为固体,则B一定是气体 | D. | B和C可能都是液体酶 |
| 药品柜编号 | ① | ② | ③ | ④ | … |
| 药品 | 氢氧化钠 氢氧化钙 | 盐酸 硫酸 | 二氧化锰 氧化铜 | 氯化钠 硫酸钠 | … |
| A. | ③和① | B. | ④和① | C. | ①和② | D. | ③和④ |
 ,已知在一定温度和相同浓度的稀溶液中,下列物质的电离程度有如下顺序:R-COOH>H2CO3>H2S>
,已知在一定温度和相同浓度的稀溶液中,下列物质的电离程度有如下顺序:R-COOH>H2CO3>H2S> >HCO3>HS.试问A跟下列哪些物质的溶液反应可得化学式为C7H5O3Na的盐( )
>HCO3>HS.试问A跟下列哪些物质的溶液反应可得化学式为C7H5O3Na的盐( )①NaOH ②Na2S ③NaHCO3 ④NaHS ⑤Na2CO3.
| A. | ③和④ | B. | ①和② | C. | ①②③⑤ | D. | 只有① |
| A. | 标准状况下,2.24LCl2溶于水,转移的电子数目为0.2NA | |
| B. | 标准状况下 11.2 L NO与11.2L O2混合,充分反应后所含分子数为0.75NA | |
| C. | 标准状况下,22.4 LCO和NO的混合气体中所含的氧原子总数为NA | |
| D. | 将含有1molFeCl3的浓溶液完全水解可得到Fe(OH)3胶粒的数目为NA |
 在一定体积的密闭容器中,进行如下化学反应:CO(g)+H2O(g)?CO2(g)+H2(g),其化学平衡常数K和温度t的关系如下表:
在一定体积的密闭容器中,进行如下化学反应:CO(g)+H2O(g)?CO2(g)+H2(g),其化学平衡常数K和温度t的关系如下表:| t℃ | 700 | 800 | 830 | 1000 |
| K | 2.6 | 1.7 | 1.0 | 0.9 |
(1)该反应的化学平衡常数表达式K=$\frac{c(C{O}_{2})×c({H}_{2})}{c(CO)×c({H}_{2}O)}$.
(2)该反应为放热反应(填“吸热”或“放热”).
(3)增加H2O(g)的浓度,CO的转化率将增大(填“增大”、“减小”或“不变”).
(4)830℃时,向该容器中加入2molCO2与2molH2,平衡时CO2的体积分数是25%.
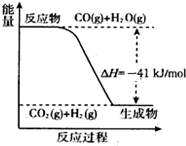
(5)已知工业制氢气的反应为CO(g)+H2O(g)?CO2(g)+H2(g),反应过程中能量变化如图所示.又已知2H2(g)+O2(g)═2H2O(g)△H=-484kJ/mol. 结合图象写出CO完全燃烧生成CO2的热化学方程式:2CO(g)+O2(g)?2CO2(g)△H=-566kJ/mol.