题目内容
【题目】硼镁泥是一种工业废料,主要成分是MgO(占40%),还有CaO、MnO、Fe2O3、FeO、Al2O3、SiO2等杂质,以此为原料制取的硫酸镁,可用于印染、造纸、医药等工业。从硼镁泥中提取MgSO4·7H2O的流程如下:
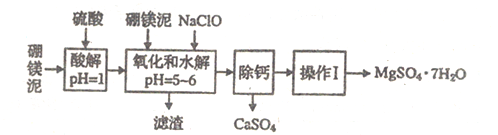
根据题意回答下列问题:
(1)实验中需用1mo/L的硫酸800mL,若用18.4mol/L的浓硫酸来配制,量取浓硫酸时,需使用的量筒的规格为____________
A.10mL B.20mL C.50mL D.100mL
(2)加入的NaClO可与Mn2+反应:Mn2++ClO-+H2O=MnO2↓+2H++Cl-,还有一种离子也会被NaClO氧化,该反应的离子方程式为_________________。
(3)滤渣的主要成分中除含有Fe(OH)3、Al(OH)3外还有________________。
(4)在“除钙”前,需检验滤波中Fe3+是否被除尽,简述检验方法:______________。
(5)已知MgSO4、CaSO4的溶解度如下表:
温度/℃ | 40 | 50 | 60 | 70 |
MgSO4 | 30.9 | 33.4 | 35.6 | 36.9 |
CaSO4 | 0.210 | 0.207 | 0.201 | 0.193 |
“除钙”是将MgSO4和CaSO4混合溶液中的CaSO4除去,根据上表数据,简要说明操作步骤: “操作Ⅰ”是将滤液继续蒸发浓缩,冷却结晶,__________,便得到了MgSO4·7H2O。
(6)实验中提供的硼镁泥共10g,得到的MgSO4·7H2O为17.22g,则MgSO4·7H2O的产率为__________________。
【答案】 D 2Fe2++C1O- +2H+=2Fe3++Cl-+H2O MnO2、SiO2 取少量滤液,向其中加入硫氰化钾容液.如果溶液不变红色.说明溶液中不含Fe3+,如果溶液变红色,说明滤液中含Fe3+ 过滤(或过滤洗涤) 70%
【解析】本题考查化学工艺流程,(1)实验室没有800mL的容量瓶,应需用要1000mL的容量瓶,因此配制硫酸时,有1000×10-3×1=V(H2SO4)×10-3×18.4,解得V(H2SO4)=54.3mL,需要的容量瓶为100mL,故选项D正确;(2)依据硼镁泥含有的成分,酸解时溶液中的离子是Mg2+、Ca2+、Mn2+、Fe3+、Fe2+、Al3+、H+、SO42-,其中Fe2+具有还原性,因此NaClO把Fe2+氧化成Fe3+,其离子反应方程式为:2Fe2++ClO- +2H+=2Fe3++Cl-+H2O;(3)根据流程图,调节pH除去的是Fe3+、Al3+,因此根据流程,滤渣的成分是Fe(OH)3、Al(OH)3、MnO2、SiO2;(4)检验Fe3+,一般用KSCN进行检验,溶液变为血红色,说明含有Fe3+,反之不含,操作是取少量滤液,向其中加入硫氰化钾容液,如果溶液不变红色,说明溶液中不含Fe3+,如果溶液变红色,说明滤液中含Fe3+ ;(5)根据溶解度与温度关系,制备MgSO4·7H2O,操作是蒸发浓缩、冷却结晶、过滤;(6)硼镁泥的质量为10g,MgO的质量分数为40%,即MgO的质量为10×40%g=4g,根据镁元素守恒,因此MgSO4·7H2O的物质的量为4/40mol=0.1mol,理论MgSO4·7H2O的质量为0.1×246g=24.6g,则产率为17.22/24.6×100%=70%。

 互动课堂系列答案
互动课堂系列答案 激活思维智能训练课时导学练系列答案
激活思维智能训练课时导学练系列答案【题目】如表所示,为提纯下列物质(括号内为少量杂质),所选用的除杂试剂与主要分离方法不正确的是
选项 | 不纯物质 | 除杂试剂与主要分离方法 |
A | 甲烷(乙烯) | 溴水 洗气 |
B | 己烷(癸烷) | 蒸馏(不需试剂) |
C | 乙酸乙酯(乙酸) | KOH溶液 分液 |
D | 蛋白质溶液(NaCl) | 水 渗析 |
A. A B. B C. C D. D
【题目】某小组同学设计如下实验,研究亚铁盐与H2O2溶液的反应。
【实验Ⅰ】试剂:酸化的0.5 mol·L-1FeSO4溶液(pH = 0.2),5% H2O2溶液(pH = 5)
操作 | 现象 |
取2mL上述FeSO4溶液于试管中,加入5滴5% H2O2溶液 | 溶液立即变为棕黄色,稍后,产生气泡。测得反应后溶液pH=0.9 |
向反应后的溶液中加入KSCN溶液 | 溶液变红 |
(1)H2O2的电子式是_______,上述实验中H2O2溶液与FeSO4溶液反应的离子方程式是________。
(2)产生气泡的原因是____________________。
【实验Ⅱ】 试剂:未酸化的0.5 mol·L-1FeSO4溶液(pH = 3),5% H2O2溶液(pH = 5)
操作 | 现象 |
取2 mL5% H2O2溶液于试管中,加入5滴上述FeSO4溶液 | 溶液立即变为棕黄色,产生大量气泡,并放热,反应混合物颜色加深且有浑浊。测得反应后溶液pH=1.4 |
(3)将上述混合物分离,得到棕黄色沉淀和红褐色胶体。取部分棕黄色沉淀洗净,加4mol·L-1盐酸,沉淀溶解得到黄色溶液。初步判断该沉淀中含有Fe2O3,经检验还含有SO42-。检验棕黄色沉淀中SO42-的方法是________。
(4)对于生成红褐色胶体的原因,提出两种假设:
i.H2O2溶液氧化Fe2+消耗H+
ii.Fe2+ 氧化的产物发生了水解
① 根据实验II记录否定假设i,理由是________。
② 实验验证假设ii:取Fe2(SO4)3溶液加热,溶液变为红褐色,pH下降,证明假设ii成立。
(5)将FeSO4溶液加入H2O2溶液后,产生红褐色胶体,反应的离子方程式是________。
【实验Ⅲ】
若用FeCl2溶液替代FeSO4溶液,其余操作与实验II相同,除了产生与II相同的现象外,还生成刺激性气味气体,该气体能使湿润的蓝色石蕊试纸变红但不褪色。
(6)产生刺激性气味气体的原因是________。
(7)由实验Ⅰ、Ⅱ、Ⅲ可知,亚铁盐与H2O2反应的现象与________(至少写两点)有关。