题目内容
(1)所需主要仪器有
(2)通过计算可知,应用托盘天平称取
(3)称量的操作顺序为(填序号)
A、调天平零点 B、游码回零 C、向小烧杯中加入碳酸钠 D、称量空烧杯
E、向右盘加砝码并把游码移到所需位置 F、将砝码回盒 G、记录称量结果
(4)若砝码和药品位置放颠倒(假设称量时未用烧杯),天平平衡时,实际称得碳酸钠的质量是
(5)下列操作使所配溶液浓度偏高的是
A.称取28.6gNa2CO3?10H2O进行配制 B.称量时用了生锈的砝码
C.往容量瓶转移溶液时,有少量液体溅出 D.碳酸钠中含有不溶性杂质
E.未洗涤溶解碳酸钠的烧杯 F.定容时,仰视刻度线
G.小烧杯洗净后未干燥即用来称量 H.容量瓶未干燥即用来配制溶液.
(2)根据n=cv计算碳酸钠的物质的量,再根据m=nM计算所需碳酸钠的质量;
(3)根据称量的实验操作过程与天平的使用解答;
(4)天平平衡原理为:m(左盘)=m(右盘)+游码读数,据此计算;
(5)分析操作对溶质的物质的量或对溶液的体积的影响,根据c=
| n |
| V |
所用仪器有托盘天平、500mL容量瓶、烧杯、玻璃棒、胶头滴管、药匙等.
容量瓶上标有刻线、温度、容量,
故答案为:托盘天平、500mL容量瓶、烧杯、玻璃棒、胶头滴管、药匙;温度;容量;
(2)需碳酸钠的物质的量为0.5L×0.2mol?L-1=0.1mol,需碳酸钠的质量为0.1mol×106g/mol=10.6g,故答案为:10.6;
(3)称量的操作顺序为:游码回零,调天平零点,称量空烧杯,记录称量结果,向右盘加砝码并把游码移到所需位置,向小烧杯中加入碳酸钠,将砝码回盒,
故答案为:BADGECF;
(4)砝码和药品位置放颠倒(假设称量时未用烧杯),实际称得碳酸钠的质量10.0g-0.6g=9.4g,故答案为:9.4;
(5)A.需碳酸钠的物质的量为0.1mol,若用Na2CO3?10H2O配制,需要Na2CO3?10H2O的质量为0.1mol×286g/mol=28.6g,无影响,故A不选;
B.用了生锈的砝码,砝码的实际质量增大,称量的碳酸钠的实际质量增大,所配溶液的浓度偏高,故B选;
C.往容量瓶转移溶液时,有少量液体溅出,移入容量瓶的碳酸钠的实际质量减小,所配溶液的浓度偏低,故C不选;
D.碳酸钠中含有不溶性杂质,称量的碳酸钠的实际质量减小,所配溶液的浓度偏低,故D不选;
E.未洗涤溶解碳酸钠的烧杯,烧杯壁上沾有少量的碳酸钠,移入容量瓶的碳酸钠的实际质量减小,所配溶液的浓度偏低,故E不选;
F.定容时,仰视刻度线,所配溶液的体积偏大,溶液浓度偏低,故F不选;
G.小烧杯洗净后未干燥即用来称量,称量的碳酸钠的实际质量减小,所配溶液的浓度偏低,故G不选;
H.配制需加水定容,容量瓶未干燥即用来配制溶液,对所配溶液浓度无影响,故H不选.
故选B.
| n |
| V |

(一) 欲配制500mL0.2mol/LNa2CO3溶液,回答下列问题:
(1)应称取 g Na2CO3·10H2O。
(2)配制该溶液所用的仪器有 ____ 。
(3)下列操作使所配溶液浓度偏低的是( )
A、容量瓶未干燥即用来配制溶液 B、往容量瓶转移溶液时有少量液体溅出
C、未洗涤溶解固体的烧杯 D、定容时,仰视刻度线
(二)某化学小组在实验室用下图提供的仪器制备溴乙烷。
已知:
①反应原理:NaBr+H2SO4(较浓)△=== NaHSO4+HBr
HBr+C2H5OHC2H5Br+H2O
②反应物用量:NaBr(S)25g,无水乙醇15mL,浓H2SO4 30mL,水15mL
③溴乙烷和乙醇的部分物理性质如下表
|
| 密度/g·mL-1 | 沸点/℃ | 溶解性 |
| 溴乙烷 | 1.461 | 38 | 难溶于水 |
| 乙醇 | 0.789 | 78 | 易溶于水 |
回答下列问题:
(4)连接上述仪器的顺序是:1接( )接( )接(4 )接( 3 )接( )(填数字)。你认为反应后溴乙烷在 (填“烧瓶”或“烧杯”)中
(5)由于浓硫酸具有强氧化性,反应产生副产物,使粗制溴乙烷常呈黄色,该副产物是 (写化学式),除去该杂质的试剂和方法是 ,为了减少该副产物的生成,根据加入的反应物,本实验采取了 _________________________________________________________的措施。
(一) 欲配制500mL0.2mol/LNa2CO3溶液,回答下列问题:
(1)应称取 g Na2CO3·10H2O。
(2)配制该溶液所用的仪器有 ____ 。
(3)下列操作使所配溶液浓度偏低的是( )
| A.容量瓶未干燥即用来配制溶液 | B.往容量瓶转移溶液时有少量液体溅出 |
| C.未洗涤溶解固体的烧杯 | D.定容时,仰视刻度线 |

已知:
①反应原理:NaBr+H2SO4(较浓)△="==" NaHSO4+HBr
HBr+C2H5OHC2H5Br+H2O
②反应物用量:NaBr(S)25g,无水乙醇15mL,浓H2SO4 30mL,水15mL
③溴乙烷和乙醇的部分物理性质如下表
| | 密度/g·mL-1 | 沸点/℃ | 溶解性 |
| 溴乙烷 | 1.461 | 38 | 难溶于水 |
| 乙醇 | 0.789 | 78 | 易溶于水 |
(4)连接上述仪器的顺序是:1接( )接( )接( 4 )接( 3 )接( )(填数字)。你认为反应后溴乙烷在 (填“烧瓶”或“烧杯”)中
(5)由于浓硫酸具有强氧化性,反应产生副产物,使粗制溴乙烷常呈黄色,该副产物是 (写化学式),除去该杂质的试剂和方法是 ,为了减少该副产物的生成,根据加入的反应物,本实验采取了 _________________________________________________________的措施。
(一) 欲配制500mL0.2mol/LNa2CO3溶液,回答下列问题:
(1)应称取 g Na2CO3·10H2O。
(2)配制该溶液所用的仪器有 ____ 。
(3)下列操作使所配溶液浓度偏低的是( )
A、容量瓶未干燥即用来配制溶液 B、往容量瓶转移溶液时有少量液体溅出
C、未洗涤溶解固体的烧杯 D、定容时,仰视刻度线
(二)某化学小组在实验室用下图提供的仪器制备溴乙烷。
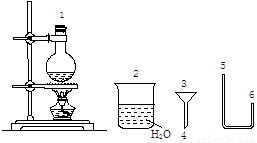
已知:
①反应原理:NaBr+H2SO4(较浓)△=== NaHSO4+HBr
HBr+C2H5OHC2H5Br+H2O
②反应物用量:NaBr(S)25g,无水乙醇15mL,浓H2SO4 30mL,水15mL
③溴乙烷和乙醇的部分物理性质如下表
|
|
密度/g·mL-1 |
沸点/℃ |
溶解性 |
|
溴乙烷 |
1.461 |
38 |
难溶于水 |
|
乙醇 |
0.789 |
78 |
易溶于水 |
回答下列问题:
(4)连接上述仪器的顺序是:1接( )接( )接( 4 )接( 3 )接( )(填数字)。你认为反应后溴乙烷在 (填“烧瓶”或“烧杯”)中
(5)由于浓硫酸具有强氧化性,反应产生副产物,使粗制溴乙烷常呈黄色,该副产物是 (写化学式),除去该杂质的试剂和方法是 ,为了减少该副产物的生成,根据加入的反应物,本实验采取了 _________________________________________________________的措施。
