题目内容
【题目】某液体化合物X2Y4 , 常用做火箭燃料.16g X2Y4在一定量的O2中恰好完全燃烧,反应方程式为X2Y4(l)+O2(g)═X2(g)+2Y2O(l).冷却后标准状况下测得气体生成物的体积为11.2L,其密度为1.25gL﹣1 , 则:
(1)反应前O2的体积V(O2)为;
(2)X2的摩尔质量为;Y元素的名称是 .
【答案】
(1)11.2L
(2)28g/mol;氢
【解析】解:(1)由方程式可知,反应前后气体的体积不发生变化,X2和氧气的关系式为1:1,故V(O2)=V(X2)=11.2L,
所以答案是:11.2L;(2)标准状况下,气体摩尔质量M=Vm×ρ,气体X2的摩尔质量=22.4L/mol×1.25g/L=28g/mol,
11.2L X2的物质的量= ![]() =0.5mol,n(X2Y4)=n(X2)=0.5mol,故Mr(X2Y4)=
=0.5mol,n(X2Y4)=n(X2)=0.5mol,故Mr(X2Y4)= ![]() =32,则Y的相对原子质量=
=32,则Y的相对原子质量= ![]() =1,故Y为氢元素,
=1,故Y为氢元素,
所以答案是:28g/mol;氢.

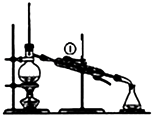
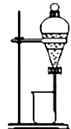
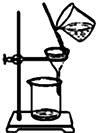
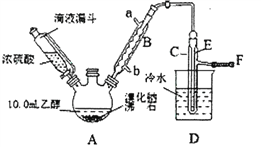
【题目】实验室用乙醇、浓硫酸和溴化钠反应来制备溴乙烷,其实验的装置如下(反应需要加热,图中省去了加热装罝):
乙醇 | 溴乙烷 | 溴 | |
状态 | 无色液体 | 无色液体 | 深红色液体 |
密度/(g cm-3) | 0.79 | 1.44 | 3. 1 |
沸点/℃ | 78.5 | 38.4 | 59 |
(1)A装置的名称是________。
(2)沸石的作用是________。
(3)己知H2SO4(浓)+NaBr![]() NaHSO4+HBr↑,写出A中生成溴乙烷的化学方程式________。
NaHSO4+HBr↑,写出A中生成溴乙烷的化学方程式________。
(4)C中收集到的粗产品混有杂质的主要成份是________;为了除去这些杂质,最好选择下列____(选填序号)溶液来洗涤所得粗产品。
A.氢氧化钠B.碘化钠C.亚硫酸钠D.碳酸氢钠
(5)粗产品洗涤、分液后,再经过蒸馏水洗涤、分液,然后加入少量的M固体,静置片刻后过滤,再将所得滤液进行蒸馏,收集到的馏分约10.0g。
①M固体的名称为________;
②在上述提纯过程中每次分液时,产品均从分液漏斗的________(填“上口”或“下口”)放出;
③从乙醇的角度考虑,本实验所得溴乙烷的产率是_________。
(6)该实验装罝的主要缺陷是________。