题目内容
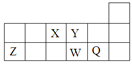
短周期元素W、X、Y、Z的原子序数依次增大,下列相关比较错误的是
| A.稳定性:H2X H2Z | B.酸性:H2ZO3<H2ZO4 |
| C.还原性:W-<Z2- | D.半径:Y3+<Z2- |
C
试题分析:短周期元素W、X、Y、Z的原子序数依次增大,X、Z的氢化物是H2X 、H2Z形式,Z在X的下一周期。同族元素从上到下,非金属性逐渐减弱,氢化物的稳定性逐渐减弱。A正确。B同种元素形成的不同价态的酸,价态越高酸性越强。正确。C非金属性X<Z,还原性:X-〉Z2-错误。D对于电子层数不同的离子,离子的电子层数越多,离子半径就越大。离子半径:Y3+<Z2-正确。

练习册系列答案
相关题目
 ⑥ DF的电子式为H∶Cl∶
⑥ DF的电子式为H∶Cl∶