题目内容
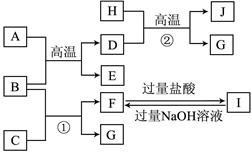
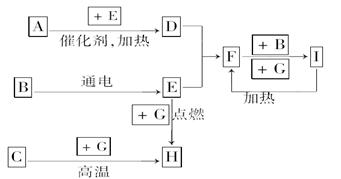
(8分)在一定条件下可实现下图所示物质之间的变化:

请填写以下空白:
(1)孔雀石的主要成分是Cu2(OH)2CO3,受热易分解。上图中的F的电子式为 。
(2)写出明矾溶液与过量NaOH溶液反应的离子方程式 。
(3)图中所得G和D都为固体,混和后在高温下可发生反应,写出该反应的化学方程式 。
(4)D与NaOH溶液反应的离子方程式为 。

请填写以下空白:
(1)孔雀石的主要成分是Cu2(OH)2CO3,受热易分解。上图中的F的电子式为 。
(2)写出明矾溶液与过量NaOH溶液反应的离子方程式 。
(3)图中所得G和D都为固体,混和后在高温下可发生反应,写出该反应的化学方程式 。
(4)D与NaOH溶液反应的离子方程式为 。
⑴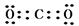 (2分)⑵Al3++4OH-=AlO2-+2H2O; (2分)
(2分)⑵Al3++4OH-=AlO2-+2H2O; (2分)
⑶3CuO +2Al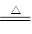 3Cu+Al2O3(2分)⑷2Al+2OH-+H2O ="=" AlO2-+3H2↑(2分)
3Cu+Al2O3(2分)⑷2Al+2OH-+H2O ="=" AlO2-+3H2↑(2分)
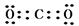 (2分)⑵Al3++4OH-=AlO2-+2H2O; (2分)
(2分)⑵Al3++4OH-=AlO2-+2H2O; (2分)⑶3CuO +2Al
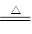 3Cu+Al2O3(2分)⑷2Al+2OH-+H2O ="=" AlO2-+3H2↑(2分)
3Cu+Al2O3(2分)⑷2Al+2OH-+H2O ="=" AlO2-+3H2↑(2分)(1)根据孔雀石的主要成分可知,其分解产物是氧化铜、CO2和水。由于A和F反应生成白色沉淀,则A是偏铝酸钠,F是CO2,生成的白色沉淀是氢氧化铝,则F的电子式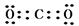 。
。
(2)由于氢氧化铝是两性氢氧化物,所以明矾和过量的氢氧化钠溶液反应的方程式是Al3++4OH-=AlO2-+2H2O。
(3)沉淀是氢氧化铝,分解得到氧化铝,氧化铝电解生成单质铝和氧气,则D是铝。由于G是氧化铜,所以二者发生铝热反应,方程式是3CuO +2Al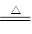 3Cu+Al2O3。
3Cu+Al2O3。
(4)铝和氢氧化钠溶液反应生成偏铝酸钠、氢气和水,反应的方程式是2Al+2OH-+H2O ="=" AlO2-+3H2↑。
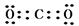 。
。(2)由于氢氧化铝是两性氢氧化物,所以明矾和过量的氢氧化钠溶液反应的方程式是Al3++4OH-=AlO2-+2H2O。
(3)沉淀是氢氧化铝,分解得到氧化铝,氧化铝电解生成单质铝和氧气,则D是铝。由于G是氧化铜,所以二者发生铝热反应,方程式是3CuO +2Al
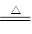 3Cu+Al2O3。
3Cu+Al2O3。(4)铝和氢氧化钠溶液反应生成偏铝酸钠、氢气和水,反应的方程式是2Al+2OH-+H2O ="=" AlO2-+3H2↑。

练习册系列答案
相关题目
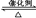 7N2+12 H2O可处理大气中的污染物NO2。当转移1.2 mol电子时,消耗的NO2在标准状况下是 L。
7N2+12 H2O可处理大气中的污染物NO2。当转移1.2 mol电子时,消耗的NO2在标准状况下是 L。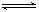 2SO3(g) ΔH="-196.6" kJ·mol-1
2SO3(g) ΔH="-196.6" kJ·mol-1