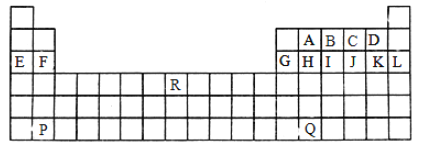
题目内容
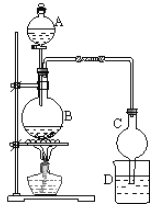
【题目】(1)某课外小组设计的实验室制取乙酸乙酯的装置如下图所示,A中盛有浓硫酸,B中盛有乙醇、乙酸,D中盛有饱和碳酸钠溶液。请回答:
①乙醇与乙酸制取乙酸乙酯的反应类型是_____。
②若用18O标记乙醇中的氧原子,则CH3CH218OH与乙酸反应的化学方程式是____。
③球形干燥管C的作用是________。
④D中选用饱和碳酸钠溶液的原因是______。
⑤反应结束后D中的现象是______。
(2)下列叙述正确的是_____(填字母)。
A.向碘水中加入酒精,萃取碘水中的碘
B.液化石油气、汽油和石蜡的主要成分都是碳氢化合物
C.用淀粉水解液做银镜反应,若有银镜产生,则证明淀粉部分水解
D.将无水乙醇和浓硫酸按体积比1:3混合,加热至140℃制取乙烯
E.相同质量的乙炔(CH≡CH)与苯分别在足量的氧气中完全燃烧,消耗氧气的物质的量相同
【答案】取代反应 ![]() 防止倒吸 乙酸乙酯与饱和Na2CO3溶液不互溶,且密度有较大差异有利于分层。饱和Na2CO3溶液还可以吸收挥发出来的乙酸的乙醇 液体分层,上层为无色油状液体 BE
防止倒吸 乙酸乙酯与饱和Na2CO3溶液不互溶,且密度有较大差异有利于分层。饱和Na2CO3溶液还可以吸收挥发出来的乙酸的乙醇 液体分层,上层为无色油状液体 BE
【解析】
(1)①乙酸和乙醇反应生成乙酸乙酯和水,该反应为酯化反应,也属于取代反应,故答案为:取代反应。
②酯化反应中酸去羟基,醇去羟基上的氢原子,也就是醇中的标记的氧原子在生成的酯中,反应方程式为:CH3COOH+C2H518OH![]() CH3CO18OC2H5+H2O,故答案为:CH3COOH+C2H518OH
CH3CO18OC2H5+H2O,故答案为:CH3COOH+C2H518OH![]() CH3CO18OC2H5+H2O。
CH3CO18OC2H5+H2O。
③从试管中出来的物质有乙酸和乙醇和乙酸乙酯,因为乙酸和乙醇易溶于水,所以用球形干燥管可以防止倒吸,故答案为:防止倒吸。
④D中选用饱和碳酸钠溶液是因为乙酸乙酯与饱和Na2CO3溶液不互溶且密度有较大差异,有利于分层;饱和Na2CO3溶液还可以吸收挥发出来的乙酸和乙醇,故答案为:乙酸乙酯与饱和Na2CO3溶液不互溶,且密度有较大差异有利于分层;饱和Na2CO3溶液还可以吸收挥发出来的乙酸的乙醇。
⑤因为乙酸乙酯是不溶于水的油状物质,所以可以看到液体分层,上层为无色油状液体,故答案为:液体分层,上层为无色油状液体。
(2)A.碘水中加入酒精不能萃取,因为酒精与水互溶,应选择苯或四氯化碳萃取,故A错误;
B.液化石油气、汽油和石蜡都是石油产品,其主要成分均是烃类,都为碳氢化合物,故B正确;
C.淀粉水解生成葡萄糖,水解液加入氢氧化钠中和酸后,再做银镜反应,若有银镜产生,说明淀粉水解,但是否全部还是部分,不能确定,故C错误;
D.制取乙烯需要加热到170℃,乙醇发生消去反应生成乙烯,加热至140℃乙醇发生分子间脱水生成乙醚,故D错误;
E. 乙炔和苯最简式都是CH,所以相同质量的乙炔与苯分别在足量的氧气中完全燃烧,消耗氧气的物质的量相同,故E正确。
故答案为:BE。