题目内容
【题目】有A、B、C、D四种短周期元素,其原子序数依次增大。A、B可形成A2B和A2B2两种化合物,B、C同主族且可形成CB2和CB3两种化合物。回答下列问题。
(1)A2B的电子式__________;A2B2的电子式__________。
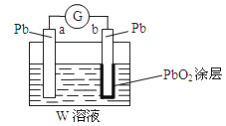
(2)CB2通入A2B2溶液中可被氧化为W,用W的溶液(体积1L,假设变化前后溶液体积变化忽略不计)组装成原电池(如右图所示)。在b电极上发生的反应可表示为:PbO2+4H++SO42-+2e-=PbSO4+2H2O,则在a电极上发生的反应可表示为__________。
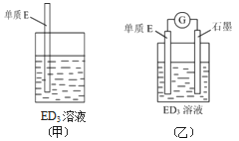
(3)金属元素E是中学化学常见元素,位于元素周期表的第四周期。该元素可与D形成ED2和ED3两种化合物。将E的单质浸入ED3溶液中,溶液由黄色逐渐变为浅绿色,该反应的离子方程式为________________________________________。
(4)依据(3)中的反应,可用单质E和石墨为电极设计一个原电池(右图),则在该原电池工作时,石墨一极发生的反应可以表示为______________________________。石墨除形成原电池的闭合回路外,所起的作用还有:________________________________________。
【答案】 ![]()
![]() Pb-2e-+SO42-=PbSO4 Fe+2Fe3+=3Fe2+ 2Fe3++2e-=2Fe2+ 充当正极材料,形成原电池,氧还分开进行
Pb-2e-+SO42-=PbSO4 Fe+2Fe3+=3Fe2+ 2Fe3++2e-=2Fe2+ 充当正极材料,形成原电池,氧还分开进行
【解析】有A、B、C、D四种短周期元素,其原子序数依次增大。A、B可形成A2B和A2B2两种化合物,B、C同主族且可形成CB2和CB3两种化合物,可以推断,B为O元素,则A为H元素,C为S元素,则D为Cl元素。
(1)H2O的电子式为![]() ;H2O2的电子式为
;H2O2的电子式为![]() ,故答案为:
,故答案为:![]() ;
;![]() ;
;
(2)SO2通入H2O2溶液中可被氧化为W,则W为H2SO4,b电极发生还原反应,则a电极发生还原反应,Pb失去电子生成PbSO4,负极电极反应式为:Pb-2e-+SO42-=PbSO4,反应的总方程式为PbO2+Pb+2H2SO4=2PbSO4+2H2O,故答案为:Pb-2e-+SO42-=PbSO4;
(3)金属元素E是中学化学常见元素,位于元素周期表的第四周期,该元素可与D形成ED2和ED3两种化合物,则E为Fe元素,将Fe浸入到FeCl3中,发生反应为Fe+2Fe3+=3Fe2+,溶液由黄色逐渐变为浅绿色,故答案为:Fe+2Fe3+=3Fe2+;
(4)石墨--铁在氯化铁电解质溶液中形成原电池,Fe为负极,失去电子生成Fe2+,负极电极反应式为:Fe-2e-=Fe2+,石墨为正极,Fe3+离子在正极获得电子生成Fe2+,正极电极反应式为:2Fe3++2e-=2Fe2+;比较甲、乙两图,说明石墨除形成闭合回路外所起的作用是:充当正极材料,形成原电池、使还原反应和氧化反应在电解质溶液中的不同区域内发生,故答案为:2Fe3++2e-=2Fe2+;充当正极材料,形成原电池、使还原反应和氧化反应在电解质溶液中的不同区域内发生。

【题目】(1)互为同分异构体的四种有机物A、B、C、D,它们的相对分子质量为74,完全燃烧只生成CO2和H2O,经分析其含氧元素的质量分数为43.3%,则这些有机物的分子式为___________,
(2)已知A、B、C、D分子结构中均含甲基,把它们分别进行下列实验以鉴别之,其实验记录如下:
| NaOH溶液 | 银氨溶液 | 新制Cu(OH)2 | 金属钠 |
A | 中和反应 | —— | 溶 解 | 产生氢气 |
B | —— | 有银镜 | 加热后有红色沉淀 | 产生氢气 |
C | 水解反应 | 有银镜 | 加热后有红色沉淀 | —— |
D | 水解反应 | —— | —— | —— |
则A、B、C、D的结构简式分别为
A____________ B____________ C____________ D____________。