题目内容
【题目】设计出燃料电池使汽油(设其成分为C5H12)氧化直接产生电流是21世纪最富有挑战性的课题之一。最近有人设计了一种固体燃料电池,固体氧化铝——氧化钇为电解质,这种固体电解质在高温下允许氧离子(O2-)在其间通过。该电池的工作原理如右图所示,其中多孔电极a、b均不参与电极反应。下列判断不正确的是
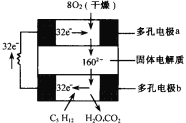
A.有O2放电的a极为电池的负极
B.b极对应的电极反应式为:C5H12+16O2--32e-=5CO2+6H2O
C.该电池的总反应方程式为:C5H12+8O2=5CO2+6H2O
D.汽油燃料电池最大的技术障碍是氧化反应不完全,产生炭粒堵塞电极的气体通道,从而使输电效能减弱
【答案】A
【解析】
A.根据图示可知通入O2的电极获得电子,发生还原反应,该电极为正极,A错误;
B.b电极汽油失去电子,发生氧化反应,电极反应式为:C5H12+16O2--32e-=5CO2+6H2O,B正确;
C.负极电极反应式为C5H12+16O2--32e-=5CO2+6H2O,正极的电极反应式为8O2+32e-=16O2-,将正极、负极电极式相加,可得总反应方程式为C5H12+8O2=5CO2+6H2O,C正确;
D.燃料电池相对于汽油直接燃烧,能量利用率高,但最大的障碍是氧化反应不完全,产生炭粒堵塞电极的气体通道,从而使输电效能减弱,D正确;
故合理选项是A。

练习册系列答案
相关题目