题目内容
(11分)甲、乙两位同学分别用不同的方法配制100mL 3.6mol/L的稀硫酸。
(1)若采用18mol/L的浓硫酸配制溶液,需要用到浓硫酸的体积为 。
(2)甲学生:量取浓硫酸,小心地倒入盛有少量水的烧杯中,搅拌均匀,待冷却至室温后转移到100 mL 容量瓶中,用少量的水将烧杯等仪器洗涤2~3次,每次洗涤液也转移到容量瓶中,然后小心地向容量瓶加入水至刻度线定容,塞好瓶塞,反复上下颠倒摇匀。
①将溶液转移到容量瓶中的正确操作是 。
②洗涤操作中,将洗涤烧杯后的洗液也注入容量瓶,其目的是__ _______。
③用胶头滴管往容量瓶中加水时,不小心液面超过了刻度,
处理的方法是_ ___(填序号)。
| A.吸出多余液体,使凹液面与刻度线相切 |
| B.小心加热容量瓶,经蒸发后,使凹液面与刻度线相切 |
| C.经计算加入一定量的浓盐酸 |
| D.重新配制 |
(4)在配制过程中如出现下列操作,所配溶液与目标溶液相比,浓度将如何变化?(用“偏大”、“偏小”或“无影响”填空)
①用量筒量取浓硫酸时仰视读数,则所配溶液的物质的量浓度______;
②定容时,仰视容量瓶刻度线,则所配溶液的物质的量浓度______;
(1)体积为20.0mL。
(2)①正确操作是 将玻璃棒插入容量瓶刻度线以下,使溶液沿玻璃棒慢慢地倒入容量瓶中 。②其目的是使溶质完全转移到容量瓶中。③处理的方法是D(填序号)。
(3)指出其中错误之处不能用量筒配制溶液,不能将水加入到浓硫酸中。
(4)①偏大;②偏小;
解析试题分析:(1)根据C1V1=C2V2得,V1=C2V2/C1=(0.1L× 3.6mol/L)/18mol/L=20.0ml,故答案为20.0mL。
(2)①若将玻璃棒插入容量瓶刻度线以上,会使少量溶液滞留在刻度线以上而导致定容时有偏差;由
于容量瓶劲较细,为避免溶液洒在外面应用玻璃棒引流,故答案为:将玻璃棒插入容量瓶刻度线以下,
使溶液沿玻璃棒慢慢地倒入容量瓶中;②洗涤液中含有部分溶质,不将洗涤液倒入容量瓶中,会导致
溶液浓度降低;③加水至离刻度线1~2cm时,用胶头滴管滴加水,容易控制水的体积,液面是凹形
的,只有液面最低端与刻度线相切时,才是溶液的真实体积,否则,会造成浓度有偏差。④用胶头滴
管往容量瓶中加水时,不小心液面超过了刻度,无论采取A.B.C的何种方式都不能配置成需要的溶
液,只能重新配置,故答案为:D;
(3)错误之处为不能用量筒配制溶液,不能将水加入到浓硫酸中。
(4)①用量筒量取浓硫酸时仰视读数,会导致量取的硫酸量偏大,故所配溶液的物质的量浓度偏大;
②定容时,仰视容量瓶刻度线,会导致量取的硫酸量偏小,故所配溶液的物质的量浓度偏小
考点:配制一定物质的量浓度的溶液

 寒假创新型自主学习第三学期寒假衔接系列答案
寒假创新型自主学习第三学期寒假衔接系列答案Ba2+是一种重金属离子,有一环境监测小组欲利用Na2S2O3、KI、K2Cr2O7等试剂测定某工厂废水中Ba2+的物质的量浓度。
(1)在容量瓶的使用方法中,下列操作不正确的是(填字母)________。
| A.使用容量瓶前检查它是否漏水 |
| B.容量瓶用水洗净后,再用待配溶液润洗 |
| C.配制溶液时,如果试样是固体,把称好的试样用纸条小心倒入容量瓶中,缓慢加水至接近标线1~2 cm处,用滴管逐滴滴加蒸馏水至标线 |
| D.配制溶液时,若试样是液体,用量筒量取试样后直接倒入容量瓶中,缓慢加水至接近标线1~2 cm处,用滴管逐滴滴加蒸馏水至标线 |
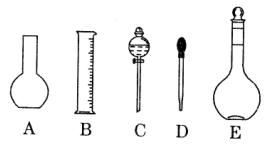
(2)现需配制250 mL 0.100 mol·L-1的标准Na2S2O3溶液,所需要的玻璃仪器除量筒、250 mL容量瓶、玻璃棒外,还需要________________。
(3)需准确称取Na2S2O3固体的质量为________g。
(4)另取废水50.00 mL,控制适当的酸度,加入足量的K2Cr2O7溶液,得到BaCrO4沉淀;沉淀经洗涤、过滤后,用适量的稀盐酸溶解,此时CrO42-全部转化为Cr2O72-;再加入过量KI溶液进行反应,然后在反应液中滴加上述标准Na2S2O3溶液,反应完全时,消耗Na2S2O3溶液36.00 mL。已知有关反应的离子方程式为①Cr2O72-+6I-+14H+=2Cr3++3I2+7H2O;②I2+2S2O32-=2I-+S4O62-。则该工厂废水中Ba2+的物质的量浓度为________。
下列说法不正确的是
| A.胶体的分散质粒子直径大小介于溶液与浊液之间 |
| B.金属冶炼通常利用氧化还原反应原理 |
| C.陶瓷、水泥和光导纤维均属于硅酸盐材料 |
| D.“煤改气”、“煤改电”等清洁燃料改造工程有利于减少雾霾天气 |
下列关于物质分类的说法正确的是
| A.金刚石、白磷都属于单质 |
| B.漂白粉、石英都属于纯净物 |
| C.氯化铵、次氯酸都属于强电解质 |
| D.葡萄糖、蛋白质都属于高分子化合物 |
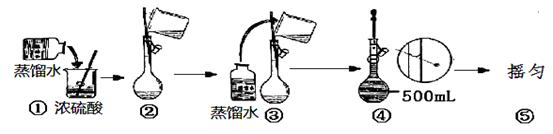

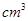 的浓硫酸的体积为:__________mL(计算
的浓硫酸的体积为:__________mL(计算