题目内容
10.化合物H是一种香料,存在于金橘中,可用如下路线合成:
已知:R-CH=CH2→(i)B2H6(ii)H2O2/OH−R-CH2CH2OH(B2H6为乙硼烷)
回答下列问题:
(1)11.2L(标准状况)的烃A在氧气中充分燃烧可以产生88g CO2和45g H2O.A的分子式是C4H10
(2)B和C均为一氯代烃,它们的名称(系统命名)分别为2-甲基-1-氯丙烷和2-甲基-2-氯丙烷
(3)在催化剂存在下1mol F与2mol H2反应,生成3-苯基-1-丙醇.F的结构简式是

(4)反应①的反应类型是消去反应;
(5)反应②的化学方程式为

(6)写出所有与G具有相同官能团的G的芳香类同分异构体的结构简式:
 、
、 、
、 、
、 .
.
分析 88gCO2为2mol,45gH2O为2.5mol,标况下11.2L烃A为0.5mol,所以烃A中含碳原子为4,H原子数为10,则A的学式为C4H10,C4H10存在正丁烷和异丁烷两种,但从框图上看,A与Cl2光照发生一氯取代时有两种产物,且在NaOH醇溶液作用下发生消去反应的产物只有一种,则A只能是异丁烷,取代后的产物为2-甲基-1-氯丙烷和2-甲基-2-氯丙烷,故D为CH2=C(CH3)2,D发生信息中的反应生成E为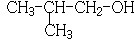 .F可以与Cu(OH)2反应,故应为醛基,与H2之间为1:2加成,则应含有碳碳双键,从生成的产物3-苯基-1-丙醇分析,F的结构简式为
.F可以与Cu(OH)2反应,故应为醛基,与H2之间为1:2加成,则应含有碳碳双键,从生成的产物3-苯基-1-丙醇分析,F的结构简式为 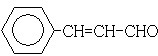 ,F中醛基氧化为羧基生成G为
,F中醛基氧化为羧基生成G为 ,D与E发生酯化反应生成H为
,D与E发生酯化反应生成H为 ,据此解答.
,据此解答.
解答 解:(1)88gCO2为2mol,45gH2O为2.5mol,标准11.2L,即为0.5mol,所以烃A中含碳原子为4,H原子数为10,则化学式为C4H10,
故答案为:C4H10;
(2)根据上面的分析可知,它们的名称(系统命名)分别为2-甲基-1-氯丙烷和2-甲基-2-氯丙烷,
故答案为:2-甲基-1-氯丙烷和2-甲基-2-氯丙烷;
(3)F可以与Cu(OH)2反应,故应为醛基,与H2之间为1:2加成,则应含有碳碳双键.从生成的产物3-苯基-1-丙醇分析,F的结构简式为 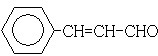 ,
,
故答案为: ;
;
(4)反应①为卤代烃在醇溶液中的消去反应,故答案为:消去反应;
(5)F被新制的Cu(OH)2氧化成羧酸G为 ,D至E为信息相同的条件,则类比可不难得出E的结构为
,D至E为信息相同的条件,则类比可不难得出E的结构为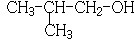 ,E与G在浓硫酸作用下可以发生酯化反应,反应方程式为:
,E与G在浓硫酸作用下可以发生酯化反应,反应方程式为: ,
,
故答案为: ;
;
(6)G中含有官能团有碳碳双键和羧基,可以将官能团作相应的位置变换而得出其芳香类的同分异构体为 、
、 、
、 、
、 ,
,
故答案为: 、
、 、
、 、
、 .
.
点评 本题有机物的推断与合成,涉及分子式的判断、反应类型、化学方程式的书写以及同分异构体的判断等,注意把握推断题的关键点和题中重要信息,积累基础知识,以及知识的综合利用.

| A. | 22.4 L N2含阿伏加德罗常数个氮分子 | |
| B. | 在标准状况下,22.4 L水的质量约为18 g | |
| C. | 22 g二氧化碳与标准状况下11.2 L HCl含有相同的分子数 | |
| D. | 标准状况下,相同体积的任何气体单质所含的原子数相同 |
| A. | 气态氢化物稳定性:HF>HCl>HBr>HI | B. | 单质氧化性:F2>Cl2>Br2>I2 | ||
| C. | 元素的非金属性:F>Cl>Br>I | D. | 离子的还原性:F->Cl->Br->I- |
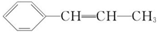
| A. | 该物质属于苯的同系物 | |
| B. | 1 mol 该物质一定条件下最多能与 1 mol H2 发生加成反应 | |
| C. | 所有碳原子可能在同一平面上 | |
| D. | 所有原子可能都在同一平面上 |
| A. | 能使溴水褪色 | B. | 能与过量的氢气充分反应生成丙醛 | ||
| C. | 不能发生银镜反应 | D. | 能被新制的氢氧化铜氧化 |
| A. | 碳酸钙和盐酸反应:CO32-+2H-═H2O+CO↑ | |
| B. | 将Fe2O3溶于稀盐酸中:Fe2O3+6H+═2Fe3++3H2O | |
| C. | 向稀盐酸溶液中加入铁粉:3Fe+6H-═3Fe3++3H2↑ | |
| D. | 把少量钠投人水中:Na+H2O═OH-+H2↑ |
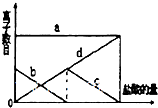 向一定量的K2CO3溶液中缓慢地滴加稀盐酸,并不断搅拌.随着盐酸的加入,溶液中离子数目也相应地发生如图变化.四条曲线与溶液中离子的对应关系,正确的是( )
向一定量的K2CO3溶液中缓慢地滴加稀盐酸,并不断搅拌.随着盐酸的加入,溶液中离子数目也相应地发生如图变化.四条曲线与溶液中离子的对应关系,正确的是( )| A. | a:Cl- b:K+ c:CO32− d:HCO3− | |
| B. | a:Cl- b:CO32− c:K+ d:HCO3− | |
| C. | a:K+ b:CO32− c:HCO3− d:Cl- | |
| D. | a:K+ b:HCO3− c:Cl- d:CO32− |

 Ⅱ.RCOOH
Ⅱ.RCOOH 、
、 .
. 、
、 .
.
 .
.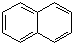 )的衍生物,且取代基都在同一个苯环上;③可发生水解反应,其中一种水解产物能发生银镜反应,另一种水解产物分子中有5种不同化学环境的氢.
)的衍生物,且取代基都在同一个苯环上;③可发生水解反应,其中一种水解产物能发生银镜反应,另一种水解产物分子中有5种不同化学环境的氢.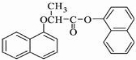 .
. ,写出以苯酚和乙醇为原料制备
,写出以苯酚和乙醇为原料制备 的合成路线流程图(无机试剂任用).合成路线流程图例如下:H2C═CH2
的合成路线流程图(无机试剂任用).合成路线流程图例如下:H2C═CH2