题目内容
【题目】(1)反应3A(g)+B(g) ===2C(g)在三种不同的条件下进行反应,在同一时间内,测得的反应速率用不同的物质表示为①vA=1 mol/(L·min)、②vC=0.5 mol/(L·min)、③vB=0.5 mol/(L·min),三种情况下该反应速率由大到小的关系是 。(用序号表示)
(2)某温度时,在一个5L的恒容容器中,X、Y、Z均为气体,三种物质的物质的量随时间的变化曲线如图所示。根据图中数据填空:
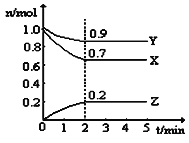
①该反应的化学方程式为__________________________。
②反应开始至2min,以气体Z表示的平均反应速率为 。
③2min反应达平衡容器内混合气体的平均相对分子质量比起始时 (填“大”,“小”或“相等”,下同),混合气体密度比起始时 。
④上述反应,在第2min时,X的转化率为 。
【答案】(1)③>①>②(2)①3X+Y![]() 2Z ② 0.02 mol·L-1·min-1 ③大;相等④30%
2Z ② 0.02 mol·L-1·min-1 ③大;相等④30%
【解析】
试题分析:(1)比较反应速率时,应该用同种物质表示不同条件下的反应速率,再进行比较,比如,可以用反应物B表示反应速率:①vB=![]() mol/(L·min)、②vB=0.25 mol/(L·min)、③vB=0.5 mol/(L·min),因此反应速率由大到小的关系为:③>①>②;
mol/(L·min)、②vB=0.25 mol/(L·min)、③vB=0.5 mol/(L·min),因此反应速率由大到小的关系为:③>①>②;
(2)①化学计量数之比等于各物质的转化量之比,即化学计量数之比为:0.3: 0.1:0.2=3:1:2,因此化学方程式为:3X+Y![]() 2Z;
2Z;
②反应开始至2min,气体Z生成0.2mol,用Z表示的平均反应速率为: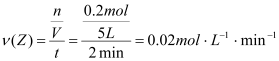 ;
;
③2min反应达平衡容器内混合气体的平均相对分子质量比起开始时大,由于混合气体的质量自始至终不变,而在固体容积中发生反应,因此混合气体的密度比起始时不变;
④在第2min时,X的转化率为:![]() ;
;

 夺冠训练单元期末冲刺100分系列答案
夺冠训练单元期末冲刺100分系列答案 新思维小冠军100分作业本系列答案
新思维小冠军100分作业本系列答案 名师指导一卷通系列答案
名师指导一卷通系列答案