题目内容
7.能作为氯、溴、碘元素非金属性(原子得电子能力)递变规律的判断依据的是( )| A. | Cl2、Br2、I2的颜色 | B. | Cl2、Br2、I2的氧化性 | ||
| C. | HCl、HBr、HI的熔点 | D. | HCl、HBr、HI的酸性 |
分析 卤族元素最外层电子数相等,但随着原子序数增大,原子半径增大,原子核对最外层电子吸引力减小,其非金属性减弱,元素的非金属性越强,其单质的氧化性越强,据此分析解答.
解答 解:卤族元素最外层电子数相等,但随着原子序数增大,原子半径增大,原子核对最外层电子吸引力减小,其非金属性减弱,元素的非金属性越强,其单质的氧化性越强,所以能作为氯、溴、碘元素非金属性(原子得电子能力)递变规律的判断依据的是Cl2、Br2、I2的氧化性,与单质的颜色、氢化物的熔沸点、氢化物的酸性强弱都无关,故选B.
点评 本题考查同一主族元素性质递变规律,明确同一主族元素原子结构与性质关系是解本题关键,氢化物的熔沸点与相对分子质量及氢键有关,与化学键强弱无关,题目难度不大.

练习册系列答案
相关题目
8.等质量的下列物质中,所含分子数最少的是( )
| A. | H2 | B. | HCl | C. | NH3 | D. | CH4 |
18.如表为元素周期表短周期的一部分.下列有关A、B、C、D、E 五种元素的叙述中正确的是( )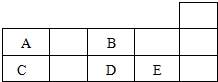

| A. | 对应阴离子的还原性:E>D | B. | 原子半径:C>B | ||
| C. | 对应氧化物的水化物的酸性:E>D | D. | A的非金属性弱于D |
15.下列有机物命名不正确的是( )
| A. | 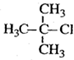 2-甲基-2-氯丙烷 2-甲基-2-氯丙烷 | B. | 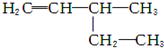 3-乙基-1-丁烯 3-乙基-1-丁烯 | ||
| C. | 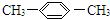 1,4-二甲苯 1,4-二甲苯 | D. | 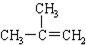 2-甲基丙烯 2-甲基丙烯 |
12.下列说法正确的是( )
| A. | CH2Cl2与C2H4Br2均无同分异构体 | B. | C2H6与C3H8一定互为同系物 | ||
| C. | 在光照条件下乙烷能使氯水褪色 | D. | 烷烃在常温下均为气态 |
19.下列物质不属于天然高分子材料的是( )
| A. | 棉花 | B. | 塑料 | C. | 蚕丝 | D. | 羊毛 |
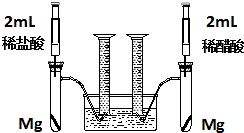 某化学小组为比较盐酸和醋酸的酸性,设计了如下实验方案.装置如图:
某化学小组为比较盐酸和醋酸的酸性,设计了如下实验方案.装置如图: 病人输液用的葡萄糖注射液是葡萄糖(化学式为C6H12O6)的水溶液,其标签上的部分内容如图所示.利用标签信息,回答下列问题(葡萄糖稀溶液的密度约为1g/cm3):
病人输液用的葡萄糖注射液是葡萄糖(化学式为C6H12O6)的水溶液,其标签上的部分内容如图所示.利用标签信息,回答下列问题(葡萄糖稀溶液的密度约为1g/cm3):