题目内容
【题目】下列反应的离子方程式书写正确的是
A.醋酸溶液与氢氧化钠反应:![]()
B.铜溶于浓硝酸:![]()
C.将过量的二氧化碳通入烧碱溶液:![]()
D.Ba(OH)2溶液与硫酸铜溶液反应:![]()
【答案】B
【解析】
A、醋酸为弱电解质,不能拆分,醋酸溶液与氢氧化钠反应的离子方程式为:CH3COOH+OH-=H2O+CH3COO-,故A错误;
B、铜与浓硝酸反应生成硝酸铜、二氧化氮、水,其离子方程式为:Cu+2NO3-+4H+=Cu2++2NO2↑+2H2O,故B正确;
C、过量的二氧化碳通入烧碱溶液,最终产物为碳酸氢钠,其反应的离子方程式为:CO2+OH-=HCO3-,故C错误;
D、Ba(OH)2溶液与硫酸铜溶液反应,生成物为硫酸钡、氢氧化铜,其离子方程式为:Ba2++SO42-+2OH-+Cu2+=BaSO4↓+Cu(OH)2↓,故D错误。

 黄冈小状元解决问题天天练系列答案
黄冈小状元解决问题天天练系列答案 三点一测快乐周计划系列答案
三点一测快乐周计划系列答案【题目】甲醇是一种新型燃料,工业上一般以CO和H2为原料合成甲醇,该反应的热化学方程式为:CO(g)+2H2(g)![]() CH3OH(g) △H1=-116kJ/mol
CH3OH(g) △H1=-116kJ/mol
(1)已知:CO(g)+![]() O2(g)=CO2 (g) △H2=-283kJ/mol
O2(g)=CO2 (g) △H2=-283kJ/mol
H2(g) +![]() O2(g)=H2O (g) △H1=-242kJ/mol
O2(g)=H2O (g) △H1=-242kJ/mol
则表示1mol气态甲醇完全燃烧生成CO2和水蒸气时的热化学方程式:________________
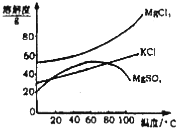
(2)在容积为1L的恒容容器中,分别研究在230℃、250℃、270℃三种温度下合成甲醇的规律。如图是上述三种温度下不同的H2和CO的起始组成比(起始时CO的物质的量均为1mol)与CO平衡转化率的关系。

请回答:
①在上述三种温度中,曲线Z对应的温度是_________
②利用图中a点对应的数据,计算出曲线Z在对应温度下CO(g)+2H2(g)=CH3OH(g)的平衡常数 K=_________。
③下列既能提高上述反应中 CO 的平衡转化率,又能增大反应速率的是____(填标号)。
a.增大压强 b.降低温度 c.增大H2浓度 d.加高效催化剂
④若上述反应在某恒温恒容容器中发生,能说明该反应达到平衡的是____(填标号)。
a.气体平均相对分子质量保持不变 b.△H1保持不变
c.![]() 保持不变 d.气体密度保持不变
保持不变 d.气体密度保持不变
(3)在某温度下,将一定量的CO和H2投入10L的密闭容器中,5min时达到平衡,各物质的物质的浓度(mol/L)变化如下表所示:
0min | 5min | 10min | |
CO | 0.1 | 0.05 | |
H2 | 0.2 | 0.2 | |
CH3OH | 0 | 0.04 | 0.05 |
若5min~10min只改变了某一条件,所改变的条件是______________。
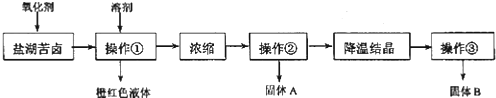
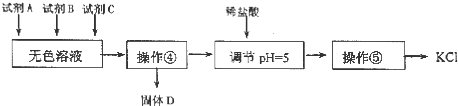
【题目】以含锂电解铝废渣(主要成分为LiF、AlF3、NaF,少量CaO等)为原料,生产碳酸锂的工艺流程如下:(已知:常温下,LiOH可溶于水,Li2CO3微溶于水)
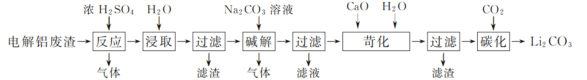
(1)含锂电解铝废渣与浓硫酸在200~400 ℃条件下反应2 h,加水浸取后过滤,得到的滤渣主要成分是________(填化学式)。
(2)流程中浸取后的过滤操作需要趁热在恒温装置中进行,否则会导致Li2SO4的收率下降,原因是________。(已知部分物质的溶解度数据见下表)
温度/℃ | Li2SO4/g | Al2(SO4)3/g | Na2SO4/g |
0 | 36.1 | 31.2 | 4.9 |
10 | 35.4 | 33.5 | 9.1 |
20 | 34.8 | 36.5 | 19.5 |
30 | 34.3 | 40.4 | 40.8 |
40 | 33.9 | 45.7 | 48.8 |
(3)40℃下进行碱解反应,得到粗碳酸锂与氢氧化铝的混合滤渣,生成氢氧化铝的离子方程式为________。
(4)苛化过程中加入的氧化钙将不溶性的碳酸锂转化成氢氧化锂溶液。若氧化钙过量,则可能会造成________。
(5)碳化反应中,CO2的吸收采用了气、液逆流的方式,这样做的优点是________。整个工艺流程中可以循环利用的物质有________。