题目内容
【题目】为了保护环境,充分利用资源,可将工业废弃物转变成重要的化工原料。回答下列问题:
(1)可用NaClO3氧化酸性FeCl2废液得到FeCl3,FeCl3具有净水作用,但腐蚀设备。
①写出NaClO3氧化酸性FeCl2的离子方程式:__________________________。
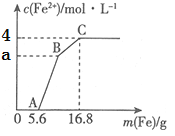
②若酸性FeCl2废液中:c(Fe2+)=2.0×10-2 mol∕L,c(Fe3+)=1.0×10-3 mol∕L,c(Cl-)=5.3×10-2 mol∕L,则该溶液的c(H+)约为_________。
③与明矾净水原理相似,FeCl3净水的原理是:________________(用恰当文字回答)
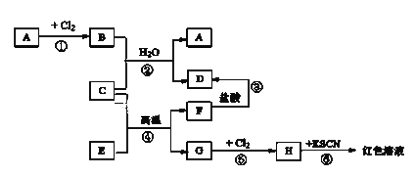
(2)可用废铁屑为原料,按下图的工艺流程制备聚合硫酸铁(PFS),PFS是一种新型的絮凝剂,处理污水比FeCl3高效,且腐蚀性小。

①酸浸时最合适的酸是______________。
②反应釜中加入的氧化剂,下列试剂中最合适的是____________(填标号)。
a.HNO3 b.KMnO4 c.Cl2 d.H2O2
③检验其中Fe2+是否完全被氧化,可选择__________(填标号)。
a.KMnO4溶液 b.Na2SO3溶液 c.KSCN溶液
【答案】ClO3-+6Fe2++6H+=Cl-+6Fe3++3H2O 10-2mol/L FeCl3在自然水中能生成Fe(OH)3胶体,Fe(OH)3胶体粒子能吸附水中的悬浮杂质 硫酸 d a
【解析】
(1)①NaClO3氧化酸性FeCl2,Cl元素的化合价从+5价降低到-1价,而Fe元素的化合价从+2价升高到+3价,结合守恒规律写出反应的离子方程式;
②根据电荷守恒:c(Cl-)=2c(Fe2+)+3c(Fe3+)+c(H+)计算;
③Fe3+水解生成的Fe(OH)3胶体粒子能吸附水中的悬浮杂质,可起到净水的作用;
(2)废铁屑在酸浸槽中加入酸,酸浸时加入的酸能腐蚀Fe且不能引进杂质,根据PFS成分知,酸为硫酸;然后过滤,向滤液中加入氧化剂,氧化剂能氧化亚铁离子且不能引进新的杂质,选取双氧水;然后向聚合釜中加入水和硫酸,最后得到PFS,结合氧化还原反应的规律分析解答。
(1)①NaClO3氧化酸性FeCl2,反应物中有氢离子参加,则生成物中有水生成,Cl元素的化合价从+5价降低到-1价,而Fe元素的化合价从+2价升高到+3价,根据得失电子守恒和电荷守恒,反应的离子方程式为:ClO3-+6Fe2++6H+=Cl-+6Fe3++3H2O,故答案为:ClO3-+6Fe2++6H+=Cl-+6Fe3++3H2O;
②根据电荷守恒:c(Cl-)=2c(Fe2+)+3c(Fe3+)+c(H+)(酸性溶液中OH-浓度很小,忽略不计),则c(H+)=c(Cl-)-2c(Fe2+)-3c(Fe3+)=1.0×10-2molL-1, 故答案为:1.0×10-2 mol/L;
③Fe3+水解生成的Fe(OH)3胶体粒子能吸附水中的悬浮杂质,水解离子方程式为Fe3++3H2O3H++Fe(OH)3,可起到净水的作用,
故答案为:Fe3+水解生成的Fe(OH)3胶体粒子能吸附水中的悬浮杂质,水解离子方程式为Fe3++3H2O3H++Fe(OH)3,可起到净水的作用;
(2)①根据实验目的制备聚合硫酸铁(PFS),酸浸时最合适的酸是稀硫酸,这样可以防止带入新的杂质,故答案为:稀硫酸;
②反应釜中加入氧化剂的作用是将Fe2+转化为Fe3+,最合适的是H2O2,这是因为利用过氧化氢做氧化剂不会带入新的杂质,故答案为:d;
③Fe2+完全被氧化为Fe3+,则溶液中不存在Fe2+,故选择KMnO4溶液检验,向溶液中滴加KMnO4溶液,高锰酸钾溶液不褪色,即可证明完全被氧化,故答案为:a。

 名校课堂系列答案
名校课堂系列答案