题目内容
将氨基甲酸铵晶体置于特制的密闭真空容器中(假设容器体积不变,固体体积忽略不计),在恒定温度下使其达到分解平衡:H2NCOONH4(s)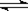 2NH3(g)+ CO2(g)。不能说明该分解反应达到平衡状态的是 ( )
2NH3(g)+ CO2(g)。不能说明该分解反应达到平衡状态的是 ( )


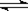 2NH3(g)+ CO2(g)。不能说明该分解反应达到平衡状态的是 ( )
2NH3(g)+ CO2(g)。不能说明该分解反应达到平衡状态的是 ( )

| A.单位时间内生成1 mol CO2的同时消耗2 mol NH3 |
| B.形成6个N—H键的同时有2个C=O键断裂 |
| C.容器中CO2与NH3的物质的量之比保持不变 |
| D.混合气体的密度不再改变的状态 |
C
试题分析:A.在任何时刻都存在单位时间内生成1 mol CO2的同时产生2 mol NH3。但是同时还消耗2 mol NH3。说明单位时间内氨气的产生速率与消耗速率相等。反应达到平衡。正确。B.在任何时刻,都存在形成6个N—H键的同时有2个C=O键形成。而现在同时还有2个C=O键断裂。说明在相同的时间内C=O键形成与断裂数目相等。反应达到平衡。正确。C.由于在反应体系中只有生成物中的CO2与NH3是气体。在任何时刻都存在容器中CO2与NH3的物质的量之比不变。因此不能作为判断平衡的标志。错误。D.参加反应的物质一固体。若反应未达到平衡,则气体的质量就要增加或减小,混合气体的密度就增大或减小,若达到平衡,则气体的质量不变,气体的密度也不再改变。因此可以证明反应达到平衡状态。

练习册系列答案
 星级口算天天练系列答案
星级口算天天练系列答案 芒果教辅达标测试卷系列答案
芒果教辅达标测试卷系列答案
相关题目
 2SO3(g),这是一个正反应放热的可逆反应。如果反应在密闭容器中进行,下述有关说法中错误的是
2SO3(g),这是一个正反应放热的可逆反应。如果反应在密闭容器中进行,下述有关说法中错误的是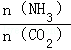 =4时,CO2的转化率随时间的变化关系如图1所示.
=4时,CO2的转化率随时间的变化关系如图1所示.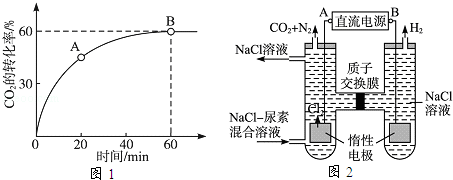
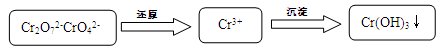
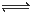 Cr2O72- + H2O
Cr2O72- + H2O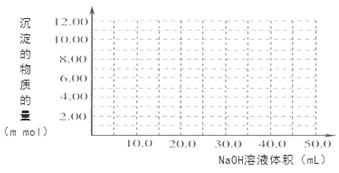
 2C(气),平衡时C的体积分数与温度和压强的关系如图所示,下列判断正确的是
2C(气),平衡时C的体积分数与温度和压强的关系如图所示,下列判断正确的是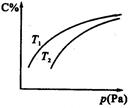
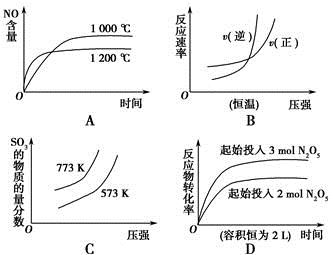
 4NO(g)+6H2O(g)ΔH=-a kJ·mol-1
4NO(g)+6H2O(g)ΔH=-a kJ·mol-1 4NO2(g)+O2(g) ΔH=+d kJ·mol-1
4NO2(g)+O2(g) ΔH=+d kJ·mol-1 2NH3 (g);△H<0。当改变某个条件并维持新条件直至新的平衡时,下表中关于新平衡与原平衡的比较正确的是
2NH3 (g);△H<0。当改变某个条件并维持新条件直至新的平衡时,下表中关于新平衡与原平衡的比较正确的是