题目内容
【题目】图中甲池的总反应式为2CH3OH+3O2+4KOH=2K2CO3+6H2O,下列说法正确的是 ( )
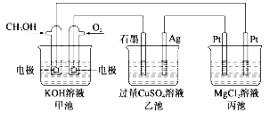
A.甲池电能转化为化学能,乙、丙池化学能转化为电能
B.甲池中通入CH3OH的电极反应式为: CH3OH-6e-+2H2O= CO+8H+
C.甲中消耗280 mL(标准状况下)O2时,丙池理论上最多产生1.45 g固体
D. 反应一段时间后,向乙池中加入一定量Cu(OH)2固体能使CuSO4溶液恢复到原浓度
【答案】C
【解析】
试题分析:A、甲池是燃料电池,是化学能转化为电能的装置,乙、丙池是电解池,是将电能转化为化学能的装置,故A错误;B、在燃料电池中,负极是甲醇发生失电子的氧化反应,在碱性电解质下的电极反应为CH3OH-6e-+2H2O+8OH-=CO32-+8H2O,故B错误;C、甲池中根据电极反应:O2+2H2O+4e-=4OH-,所以消耗280mL(标准状况下0.0125mol)O2,则转移电子0.05mol,根据丙装置中,在阴极上是氢离子放电,减小的氢离子是0.025mol,所以镁离子和氢氧根离子之间反应生成氢氧化镁,理论上最多产生氢氧化镁质量应该是0.125×2mol×58g/mol=1.45g固体,故C正确;D、电解池乙池中,电解后生成硫酸、铜和氧气,要想复原,要加入氧化铜,故D错误。

【题目】化学反应速率和限度与生产、生活密切相关.
(1)某学生为了探究锌与盐酸反应过程中的速率变化,在400mL稀盐酸中加入足量的锌粉,用排水法收集反应放出的氢气,实验记录如下(累计值):
时间 | 1 | 2 | 3 | 4 | 5 |
氢气体积/mL(标况) | 100 | 240 | 464 | 576 | 620 |
①哪一段时间内反应速率最大:____min(填“0~1”“1~2”“2~3”“3~4”或“4~5”)。
②3~4min内以盐酸的浓度变化来表示的该反应速率______(设溶液体积不变)。
(2)另一学生为控制反应速率防止反应过快难以测量氢气体积.他事先在盐酸中加入等体积的下列溶液以减慢反应速率但不影响生成氢气的量.你认为不可行的是____(填字母)。
A 蒸馏水 B KCl洛液 C 浓盐酸 D CuSO4溶液
(3)在4L密闭容器中,X、Y、Z三种气体的物质的量随时间变化曲线如图。

①该反应的化学方程式是_______________。
②该反应达到平衡状态的标志是___________(填字母)。
A Y的体积分数在混合气体中保持不变 B X,、Y的反应速率比为3:1
C 容器内气体压强保持不变 D 容器内气体的总质量保持不变
E 生成1molY的同时消耗2molZ
③2min内Y的转化率为__________。
