��Ŀ����
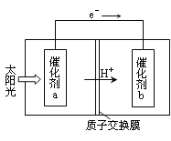
����Ŀ����I��CuCl2��Һ��_____�ԣ������ǣ������ӷ���ʽ��ʾ��____________
��II��BaSO4��Һ�д���______ƽ�⣬�����ʽΪ��__________________
��III����֪����2CH3OH��l��+3O2��g���T2CO2��g��+4H2O��g����H1=��1275.6kJ/mol
��2CO��g��+O2��g���T2CO2��g����H2=��566.0kJ/mol��
��H2O��g���TH2O��l����H3=��44.0kJ/mol
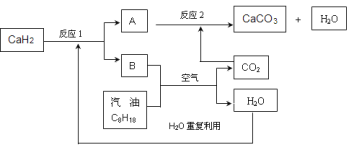
����������Ӧ�У���S��0����___________���״�ȼ������һ����̼��Һ̬ˮ���Ȼ�ѧ����ʽ��______________________
��IV����֪̼��H2CO3��Ka1=4.3��10-7��Ka2=5.6��10-11
����H2C2O4��Ka1=5.9��10-2��Ka2=6.4��10-5��0.1 mol/L Na2CO3��Һ��pH____________0.1 mol/L Na2C2O4��Һ��pH����ѡ����ڡ���С�ڡ����ڡ�������Ũ�Ȳ�����Һ��̼����Һ�У�������Ũ�Ƚϴ����___________��������Ũ�ȵIJ�����Һ��̼����Һ�������ϣ���Һ�и�������Ũ�ȴ�С��˳����ȷ����_____����ѡ���ţ�
A��c��H+��>c��HC2O4-��>c��HCO3-��>c��CO32-��
B��c��HCO3-��>c��HC2O4-��c��C2O42-��>c��CO32-��
C��c��H+��>c��HC2O4-��>c��C2O42-��>c��CO32-��
D��c��H2CO3��>c��HCO3-��>c��HC2O4-��>c��CO32-��
���𰸡� �� Cu2++2H2O Cu(OH)2+2H+ �ܽ� BaSO4��S�� Ba2+��aq��+SO42-��aq�� �ڢ� CH3OH��l��+O2��g��==CO��g��+2H2O��l����H=��442.8kJ/mol�� ���� ���ᣨH2C2O4�� AC
��������(I)CuCl2����ǿ�������Σ�ˮ�����Һ�����ԣ����ӷ���ʽΪCu2++2H2O Cu(OH)2+2H+���ʴ�Ϊ���Cu2++2H2O Cu(OH)2+2H+��
(II)BaSO4��Һ�д����ܽ�ƽ�⣬ƽ�ⷽ��ʽΪBaSO4(S) Ba2+(aq)+SO42-(aq)���ʴ�Ϊ���ܽ⣻ BaSO4(S) Ba2+(aq)+SO42-(aq)��
(III) ��������ʵ���Խ����SԽ�����ʵ���ʱ�����ʵ��أ�����С��Һ��С�����壬���������Ӧ�У���S��0���Тںۣ͢����ݢ�2CH3OH(l)+3O2(g)�T2CO2(g)+4H2O(g)��H=-1275.6kJmol-1����2CO(g)+O2(g)�T2CO2(g)��H=-566.0kJmol-1����H2O(g)�TH2O(l)��H=-44.0kJmol-1�����ݸ�˹���ɣ�����֪��Ӧ![]() ��(��-��+����4)�õ�CH3OH(l)+O2(g)=CO(g)+2H2O(l)�����Ը÷�Ӧ����H=
��(��-��+����4)�õ�CH3OH(l)+O2(g)=CO(g)+2H2O(l)�����Ը÷�Ӧ����H=![]() ��[(-1275.6kJ/mol)-(-566.0kJ/mol)+(-44.0kJ/mol)��4]=-442.8kJmol-1����CH3OH(l)+O2(g)=CO(g)+2H2O(l)��H=-442.8kJmol-1���ʴ�Ϊ���ڢ���CH3OH(l)+O2(g)=CO(g)+2H2O(l)��H=-442.8kJmol-1��
��[(-1275.6kJ/mol)-(-566.0kJ/mol)+(-44.0kJ/mol)��4]=-442.8kJmol-1����CH3OH(l)+O2(g)=CO(g)+2H2O(l)��H=-442.8kJmol-1���ʴ�Ϊ���ڢ���CH3OH(l)+O2(g)=CO(g)+2H2O(l)��H=-442.8kJmol-1��
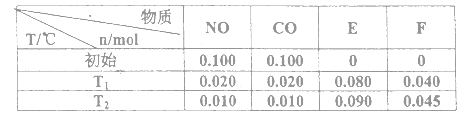
(IV)����ĵڶ�������ƽ�ⳣ������̼��ĵڶ�������ƽ�ⳣ��������ƽ�ⳣ��ԽС����������ӵ�ˮ��̶�Խ������̼������ӵ�ˮ��̶ȴ��ڲ�������ӣ�0.1mol/L Na2CO3��Һ��pH����0.1mol/L Na2C2O4��Һ��pH�����������ǿ��̼�ᣬ���Ũ�Ȳ�����Һ��̼����Һ�У�������Ũ�Ƚϴ���Dz��ᣬ����Ķ������볣��������̼��ģ����Բ���ĵ���̶ȴ���̼�ᣬ��̼���Ե�һ������Ϊ���������Һ��c(H+)>c(HC2O4-)> c(C2O42-)> c(HCO3-)> c(CO32-)����AC��ȷ��BD���ʴ�Ϊ�����ڣ���� AC��

 �������¿��ÿ�ʱ��ҵϵ�д�
�������¿��ÿ�ʱ��ҵϵ�д� Ӣ�żƻ�ͬ����ʱ��Чѵ��ϵ�д�
Ӣ�żƻ�ͬ����ʱ��Чѵ��ϵ�д�