题目内容
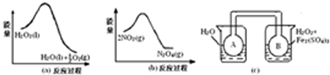
12.1mol Cl2与Ca(OH)2完全反应,转移的电子数是2NA错误 (判断对错)分析 反应2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H20中只有Cl元素化合价发生变化,分别由0价变化为-1价、+1价,以此解答该题.
解答 解:Cl元素化合价由0价变化为-1价、+1价,若有1molCl2参加反应,则转移1mol电子,转移的电子数是NA,故答案为:错误.
点评 本题考查氧化还原反应,为高频考点,侧重于学生的分析能力的考查,注意元素化合价的变化,为解答该类题目的关键,难度不大.

练习册系列答案
相关题目
20.NA代表阿伏加德罗常数的值.下列叙述正确的是( )
| A. | 1.0 L 1.0 mo1•L-1的NaAlO2 水溶液中含有的氧原子数为2 NA | |
| B. | 密闭容器中2 mol NO与1 mol O2充分反应,产物的分子数为2 NA | |
| C. | 过氧化钠与水反应时,生成0.1 mol 氧气转移的电子数为0.2 NA | |
| D. | 标准状况下,33.6 L氟化氢中含有氟原子的数目为1.5 NA |
7.用NA表示阿伏加德罗常数的值.下列叙述中不正确的是( )
| A. | 分子总数为NA的NO2和CO2混合气体中含有的氧原子数为2NA | |
| B. | 28g乙烯(C2H4)和环丁烷(C4H8)的混合气体中含有的碳原子数为2NA | |
| C. | 常温常压下,92g的NO2和N2O4混合气体含有的原子总数为6NA | |
| D. | 17gOH-中含有的质子数为10NA |
17.汽车安全气囊碰撞时会发生如下反应:10NaN3+2KNO3=5Na2O+X+16N2↑,则下列说法正确的是( )
| A. | X的化学式为:K2O2 | B. | KNO3发生氧化反应 | ||
| C. | NaN3的电子式为 | D. | 氧化产物与还原产物质量比为1:15 |
1.现有a、b、c、d四种金属片,①若将a、b用导线连接后浸入稀硫酸,b上有气泡产生;②若将c、d用导线连接浸入稀硫酸,c发生氧化反应;③若将b、c用导线连接浸入稀硫酸,电子的方向是:b→c.则下列说法正确的是( )
| A. | 金属的活泼顺序为:a>c>b>d | |
| B. | 在①的溶液中,SO42-向b极移动 | |
| C. | 在③的装置中,一段时间后b电极质量将会减轻 | |
| D. | 二次电池放电时的反应和充电时的反应是可逆反应 |
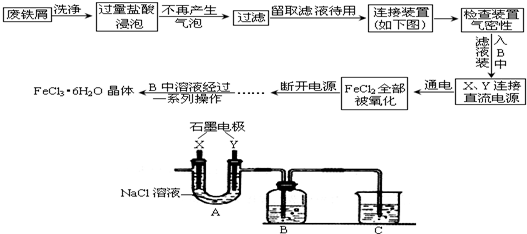
 ;检验元素X、Y、Z以质量比为1:7:12形成的化合物中所含阳离子的离子反应方程式是:
;检验元素X、Y、Z以质量比为1:7:12形成的化合物中所含阳离子的离子反应方程式是: