题目内容
相同温度下,体积均为0.25 L的两个恒容密闭容器中发生可逆反应:X2(g)+3Y2(g)?2XY3(g);△H=-92.6kJ?mol-1,实验测得反应起始时、达到平衡状态时的有关数据如下表所示,不正确的是( )
| ||||||||||||||||||
分析:(A)、由达平衡时①放出的热为23.15 kJ,计算平衡时XY3的物质的量浓度,再根据两平衡是完全等效平衡解答;
(B)、平衡常数只与温度有关;
(C)、由达平衡时①放出的热为23.15 kJ,计算平衡时X2、Y2和XY3的物质的量,分析②是否处于平衡状态或是向哪个方向进行,判断②是吸热还是放热,再根据转化率计算具体的值;
(D)、从平衡移动的角度比较反应放出的热量与23.15kJ的关系.
(B)、平衡常数只与温度有关;
(C)、由达平衡时①放出的热为23.15 kJ,计算平衡时X2、Y2和XY3的物质的量,分析②是否处于平衡状态或是向哪个方向进行,判断②是吸热还是放热,再根据转化率计算具体的值;
(D)、从平衡移动的角度比较反应放出的热量与23.15kJ的关系.
解答:解:A、①容器中放出23.15kJ热量,则生成氨气的物质的量为:
×2mol=0.5mol,利用三段式法计算:
?N2(g)+3H2(g) 2NH3(g)
2NH3(g)
起始:1mol 3mol 0
转化:0.25mol 0.75mol 0.5mol
平衡:0.75mol 2.25mol 0.5mol
此时XY3的物质的量浓度均为
=2 mol/L,
将②按化学计量数比换算成左边与①对应的物质的物质的量相等,恒温恒容下,两平衡是完全等效平衡,平衡时各物质的浓度相等,故A正确;
B、平衡常数只与温度有关,温度不变,对同一反应平衡常数不变,故B正确;
C、由上述计算,可知平衡时①容器中X2、Y2和XY3的物质的量分别为0.75mol、2.25mol和0.5mol,②与①为完全等效平衡,所以,平衡时②容器中X2、Y2和XY3的物质的量也分别为0.75mol、2.25mol和0.5mol,可知②的反应向逆反应方向进行,反应过程需要吸收热,故C错误;
D、若容器①体积为0.20L,增大压强平衡向正反应方向移动,放出热量多,D项正确.
故选C.
| 23.15KJ |
| 92.6KJ |
?N2(g)+3H2(g)
 2NH3(g)
2NH3(g)起始:1mol 3mol 0
转化:0.25mol 0.75mol 0.5mol
平衡:0.75mol 2.25mol 0.5mol
此时XY3的物质的量浓度均为
| 05mol |
| 0.25L |
将②按化学计量数比换算成左边与①对应的物质的物质的量相等,恒温恒容下,两平衡是完全等效平衡,平衡时各物质的浓度相等,故A正确;
B、平衡常数只与温度有关,温度不变,对同一反应平衡常数不变,故B正确;
C、由上述计算,可知平衡时①容器中X2、Y2和XY3的物质的量分别为0.75mol、2.25mol和0.5mol,②与①为完全等效平衡,所以,平衡时②容器中X2、Y2和XY3的物质的量也分别为0.75mol、2.25mol和0.5mol,可知②的反应向逆反应方向进行,反应过程需要吸收热,故C错误;
D、若容器①体积为0.20L,增大压强平衡向正反应方向移动,放出热量多,D项正确.
故选C.
点评:本题考查化学平衡移动问题、等效平衡、反应热等问题,题目难度不大,注意C项根据计算分析,多认为无法判断是吸热还是放热.

练习册系列答案
 轻松课堂单元期中期末专题冲刺100分系列答案
轻松课堂单元期中期末专题冲刺100分系列答案
相关题目
| (2009?南通二模)相同温度下,体积均为0.25L的两个恒容密闭容器中发生可逆反应: N2(g)+3H2(g)?2NH3(g)△H=-92.6kJ/mol.实验测得起始、平衡时的有关数据如下表:
| ||||||||||||||||||
在相同温度下,体积均为1L的四个密闭容器中,保持温度和容积不变,以四种不同的投料方式进行反应.平衡时有关数据如下(已知2SO2(g)+O2(g)?2SO3(g)△H=-196.6kJ?mol-1).
|
相同温度下,体积均为0.25L的两个恒容密闭容器中发生可逆反应:X2(g)+3Y2(g)?2XY3(g)△H=-92.6kJ?mol-1起始时各物质物质的量如下表所示:
达到平衡后,①容器中XY3的物质的量为0.5mol.下列叙述正确的是( )
| 容器 编号 |
起始时各物质物质的量/mol | ||
| X2 | Y2 | XY3 | |
| ① | 1 | 3 | 0 |
| ② | 0.6 | 1.8 | 0.8 |
| A、容器①、②中反应的平衡常数不相等 |
| B、达平衡时,容器②中 XY3的物质的量浓度为2mol?L-1 |
| C、容器①中反应达到平衡时放出的热量为23.15kJ |
| D、容器②中反应达到平衡时放出热量 |
相同温度下,体积均为0.5L的两个恒容密闭容器中发生可逆反应:A(g)+2B(g)?xC(g)△H=-64kJ?mol-1实验测得反应在起始、达到平衡时的有关数据如下表所示.下列叙述错误的是( )
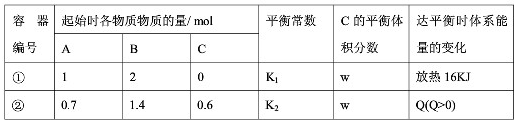

| A、x=2 | B、容器①、②中反应的平衡常数K1=K2 | C、若容器①体积为0.4L,则达平衡时放出的热量可能仍为16kJ | D、达平衡时,两个容器中C的物质的量浓度均为1mol.L-1 |