��Ŀ����
����Ŀ����.��������������Ԫ��,�̷�(FeSO4��7H2O)������ȱ����ƶѪҩƷ����Ҫ�ɷ֡�
(1)FeSO4��Һ�ڿ����л����������ʲ������ɫ����,�䷢����Ӧ�����ӷ���ʽ��__________;ʵ����������FeSO4��Һʱ������____�Է�ֹ�䱻�������������һ��ʵ��֤��FeSO4��Һ�Ƿ�����__��
��.���������[(NH4)2Fe(SO4)2��6H2O]�������������ױ���������,�����ڴ�������������
(2)��������鱗��ױ�������ԭ����______________________��
(3)Ϊ����ֽ����ijɷ�,�������ʵ��װ�ý���ʵ��,����A�е�������������ֽ���ȫ��

��A�й����ּ��Ƚϳ�ʱ���,ͨ�뵪��,Ŀ����_____________________________��
��װ��B��BaCl2��Һ��������Ϊ�˼���ֽ�������Ƿ���SO3��������,�����и�����,�۲쵽������Ϊ_��
��ʵ����,�۲쵽C���а�ɫ��������,��C�з����ķ�ӦΪ___________ (�����ӷ���ʽ��ʾ)��
���𰸡���.(1)12Fe2++3O2+6H2O=Fe(OH)3��+8Fe3+(����������Ҳ����) ���� ȡ����FeSO4��Һ���Թ���,������KSCN��Һ,�����Һ���,��˵��FeSO4��Һ�ѱ�����,�粻���,��˵��FeSO4��Һû�б�������
��.(2)�����������Һ��N![]() ����ˮ������c(H+),������Fe2+������Ӧ�Ľ��С�
����ˮ������c(H+),������Fe2+������Ӧ�Ľ��С�
(3)��ʹ�ֽ������������B��C�б����ճ��
����Һ�����(����ְ�ɫ����)
��SO2+H2O2+Ba2+=aSO4��+2H+(��SO2+H2O2=H++S![]() ��S
��S![]() +Ba2+=aSO4��)
+Ba2+=aSO4��)
��������
(1)Fe2+��O2����ΪFe3+,�������ɺ��ɫ��Fe(OH)3����;�������ۿ��Է�ֹFe2+������ΪFe3+;ͨ����KSCN����Fe3+��
(2)N![]() ˮ��������,c(H+)Խ��,��Ӧ4Fe2++O2+10H2O=Fe(OH)3��+8H+������еij̶�ԽС,Fe2+Խ���ױ�������
ˮ��������,c(H+)Խ��,��Ӧ4Fe2++O2+10H2O=Fe(OH)3��+8H+������еij̶�ԽС,Fe2+Խ���ױ�������
(3)��ͨ��N2���Խ�װ���е�����ȫ���ŵ�B��C,��֤����ȫ���ա�
��SO2����BaCl2��Ӧ,��SO3���Ժ�BaCl2��Ӧ����BaSO4������
��H2O2��SO2����ΪS![]() ,����Ba2+��Ӧ����BaSO4������
,����Ba2+��Ӧ����BaSO4������

����Ŀ��5�ֹ�������A��B��C��D��E���±��в�ͬ������������ɣ����Ǿ�������ˮ��
������ | Na+�� Al3+ Fe3+�� Cu2+����Ba2+ |
������ | OH����Cl����CO32����NO3����SO4�� |
�ֱ�ȡ���ǵ�ˮ��Һ����ʵ�飬������£�
��A��Һ��C��Һ��Ϻ������ɫ��������ó����м�������ϡHNO3�����������ܽ⣬ʣ���ɫ���壻
��B��Һ��E��Һ��Ϻ�������ɫ������ͬʱ�����������壻
������C��Һ��D��Һ��Ϻ������ɫ����������C��Һ��D��Һ��Ϻ�������
��B��Һ��D��Һ��Ϻ�������
�ݽ�38.4 g CuƬͶ��װ������D��Һ���Թ��У�CuƬ���ܽ⣬�ٵμ�1.6 mol��L��1ϡH2SO4��Cu���ܽ⣬�ܿڸ����к���ɫ������֡�
��1���ݴ��ƶ�A��C�Ļ�ѧʽΪ��A______________��C______________��
��2��д��������з�����Ӧ�Ļ�ѧ����ʽ____________________________________��
��3��D��Һ�е���ʯ����Һ��������___________________________________________��ԭ����_____________________________________________(�����ӷ���ʽ˵��)��
��4�����������Ҫ��CuƬ��ȫ�ܽ⣬���ټ���ϡH2SO4�������____________mL��
��5������500 mL 3 mol��L��1��E��Һ�������11.2 L CO2����(��״�� ��)����Ӧ����Һ�и����ӵ�������Ũ����С�����˳��Ϊ_________________________________��
��6�����ö��Ե缫���A��B�Ļ����Һ�����ʵ����ʵ�����Ϊ0.1 mol����������ϵ�л���ͨ�������������������(��״����)V��ͨ�����ӵ����ʵ���n�Ĺ�ϵ(��������������ˮ)��_________
 ����
����
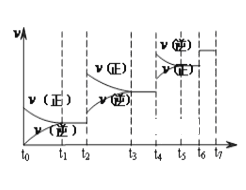
����Ŀ����l0��ʱ��10 mL 0.4 mol L��1H2O2��Һ�������ֽ⣺2H2O2![]() 2H2O��O2������ͬʱ�̲������O2�������������Ϊ��״�������±���
2H2O��O2������ͬʱ�̲������O2�������������Ϊ��״�������±���
t/min | 0 | 2 | 4 | 6 |
V(O2)/mL | 0.0 | 9.9 | 17.2 | 22.4 |
������������ȷ���ǣ���Һ����仯���Բ��ƣ�
A. 0��2 min��ƽ����Ӧ���ʱ�4��6 min��
B. 0��6 min ��ƽ����Ӧ����v(H2O2)��3.3��10��2 moL��1 L��1 min��1
C. ��Ӧ�� 6 min ʱ��c(H2O2)��0.3 mol��L��1
D. ��Ӧ��6 minʱ��H2O2�ֽ���50%
����Ŀ����1��һ���¶��£�Ksp[Mg3��PO4��2]��6.0��10��29��Ksp[Ca3��PO4��2]��6.0��10��26����Ũ�Ⱦ�Ϊ0.20mol��L��1��MgCl2��CaCl2�����Һ����μ���Na3PO4��������________�������ѧʽ�����������Һ����һ�ֽ��������ӳ�����ȫ��Ũ��С��10��5mol��L��1��ʱ����Һ�е���һ�ֽ��������ӵ����ʵ���Ũ��Ϊ________��
��2������ʯ����Ҫ�ɷ�BaCO3����Ca2����Mg2����Fe3�������ʣ���ʵ�������ö���ʯ�Ʊ�BaCl2��2H2O���������£�
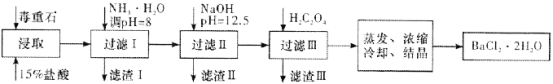
�ٶ���ʯ�������ȡǰ������ĥ��Ŀ����________��
�ڼ���NH3��H2O����pH��8�ɳ�ȥ________�������ӷ��ţ����������к�________���ѧʽ��������H2C2O4ʱӦ���������ԭ����________��
Ca2�� | Mg2�� | Fe3�� | |
��ʼ����ʱ��pH | 11.9 | 9.1 | 1.9 |
��ȫ����ʱ��pH | 13.9 | 11.1 | 3.7 |
��֪��Ksp��BaC2O4����1.6��10��7��Ksp��CaC2O4����2.3��10��9��
��3����֪25��ʱ��CaSO4��ˮ�еij����ܽ�ƽ��������ͼ��ʾ����100mL�������µ�CaSO4������Һ�м���400mL 0.01mol��L��1 Na2SO4��Һ������������ȷ����___������ĸ����
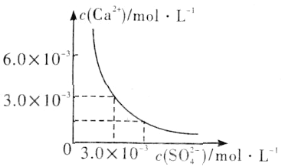
A����Һ������CaSO4������������Һ��c(SO42��)��ԭ���Ĵ�
B����Һ��������������Һ��c��Ca2������c(SO42��)����С
C����Һ������CaSO4��������Һ��c��Ca2������c(SO42��)����С
D����Һ��������������������Һ��c(SO42��)��ԭ���Ĵ�