题目内容
在一种烧碱溶液中混有少量纯碱(杂质浓度〈0.1mol•L-1)。某同学欲测定其中氢氧化钠的物质的量浓度。现有的药品和仪器有:药品:①0.10mol•L-1盐酸 ②0.10mol•L-1Ba(OH)2溶液 ③0.10mol•L-1BaCl2溶液④酚酞试液 ⑤甲基橙试液仪器:①铁架台(带滴定管夹) ②烧杯 ③酸、碱式滴定管 ④锥形瓶 ⑤玻璃棒 ⑥过滤装置根据现有的药品和仪器(量和规格均能满足要求),你认为能测定就只回答A组问题,认为不能测定就只回答B组问题。A组问题:
(1)指出所选用的试剂(写编号)________。
(2)实验过程中有关反应的离子方程式________。
(3)简述你的操作步骤。
B组问题:
(1)试说明不能测定的原因________。
(2)指出需要补加的试剂名称________。
(3)简述你的操作步骤。
答案:
解析:
解析:
| A组问题:(1)①、③、④或⑤
(2)Ba2++CO2-3══BaCO3↓H++OH+══H2O (3)用碱式滴定管取一定体积的混合溶液,先加入过量BaCl2溶液,使Na2CO3完全转变为BaCO3沉淀,过滤后以酚酞作指示剂,以0.10mo1L-1盐酸作标准溶液,用酸式滴定管进行滴定,并计算。
|

练习册系列答案
相关题目
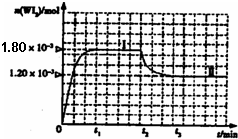 (2010?枣庄一模)卤素单质的性质活泼,卤素的化合物应用广泛,研究卤素单质及其化合物具有重要意义.
(2010?枣庄一模)卤素单质的性质活泼,卤素的化合物应用广泛,研究卤素单质及其化合物具有重要意义.
