题目内容
【题目】(1)Cu+基态核外电子排布式为__________。
(2)基态Fe原子有______个未成对电子,Fe3+的电子排布式为__________。
(3)S的基态原子核外有_____个未成对电子;Si的基态原子核外电子排布式为_______________。
(4)Cu的价层电子轨道示意图为_____。
(5)基态Si原子中,电子占据的最高能层符号为_____,该能层具有的原子轨道数为_____,电子数为_____。
【答案】[Ar]3d10(或1s22s22p63s23p63d10) 4 1s22s22p63s23p63d5 2 1s22s22p63s23p2 ![]() M 9 4
M 9 4
【解析】
(1)铜是29号元素,Cu+基态核外电子排布式为[Ar]3d10(或1s22s22p63s23p63d10)。
故答案为:[Ar]3d10(或1s22s22p63s23p63d10);
(2)Fe是26号元素,基态Fe原子核外电子排布为1s22s22p63s23p63d64s2,3d能级中有4个未成对电子,Fe3+的电子排布式为1s22s22p63s23p63d5。故答案为:4 ;1s22s22p63s23p63d5;
(3)S的电子排布式为1s22s22p63s23p4,S的基态原子核外3p能级有2个未成对电子;Si核外有14个电子,Si的基态原子核外电子排布式为1s22s22p63s23p2。故答案为:2;1s22s22p63s23p2;
(4)铜为29号元素,Cu基态核外电子排布式为[Ar]3d104s1(或1s22s22p63s23p63d104s1),Cu的价层电子轨道示意图为![]() 。故答案为:
。故答案为:![]() ;
;
(5)基态Si原子中,电子占据K、L、M三个能层,电子数分别是2、8、4,最高能层符号为M,该能层具有的原子轨道数为3s有1个,3p有3个,3d有5个,共9个轨道,电子数为4。故答案为:M; 9;4。

【题目】某化学小组采用类似制乙酸乙酯的装置(如图),以环己醇制备环己烯。
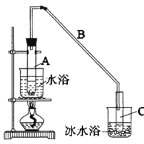
已知: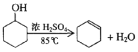
密度(g/cm3) | 熔点(℃) | 沸点(℃) | 溶解性 | |
环已醇 | 0.96 | 25 | 161 | 能溶于水 |
环已烯 | 0.81 | -103 | 83 | 难溶于水 |
(1)制备粗品
将12.5mL环己醇加入试管A中,再加入lmL浓硫酸,摇匀后放入碎瓷片,缓慢加热至反应完全,在试管C内得到环己烯粗品。
①A中碎瓷片的作用是:_______________,导管B除了导气外还具有的作用是:_______________。
②试管C置于冰水浴中的目的是。:_______________
(2)制备精品
①环己烯粗品中含有环己醇和少量酸性杂质等。加入饱和食盐水,振荡、静置、分层,环己烯在:_______________层(填上或下),分液后用:_______________ (填入编号)洗涤。
a.KMnO4溶液b.稀H2SO4c.Na2CO3溶液