题目内容
200 mL 2 mol·L-1的NaCl溶液(ρ=1.10 g·mL-1)在铜电极的电解池中于不断搅拌下进行电解。当在阴极上有22.4 L(标准状况下)的气体放出时停止电解。电解后溶液中NaCl的质量分数为
- A.12.72%
- B.7.96%
- C.8.30%
- D.无法计算
这是一道重在考查考生审题能力、分析能力的习题,要求考生在审题时注意到铜电极和惰性电极的差异。用铜电极电解NaCl溶液时,阳极反应式:Cu-2e-
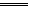 Cu2+,阴极反应式:2H++2e-
Cu2+,阴极反应式:2H++2e- Cu(OH)2↓+H2↑。可见,对原NaCl溶液损失的仅是水。由反应式可知阴极上生成22.4 L H2时消耗的H2O为2 mol,即36 g。电解前m〔NaCl(aq)〕=1.10 g·mL-1×200 mL="220" g,电解后m〔NaCl(aq)〕="220" g-36 g="184" g,n(NaCl)="2" mol·L-1×0.2 L=0.4 mol,m(NaCl)=0.4 mol×58.5 g·mol-1=23.4 g。
Cu(OH)2↓+H2↑。可见,对原NaCl溶液损失的仅是水。由反应式可知阴极上生成22.4 L H2时消耗的H2O为2 mol,即36 g。电解前m〔NaCl(aq)〕=1.10 g·mL-1×200 mL="220" g,电解后m〔NaCl(aq)〕="220" g-36 g="184" g,n(NaCl)="2" mol·L-1×0.2 L=0.4 mol,m(NaCl)=0.4 mol×58.5 g·mol-1=23.4 g。w(NaCl)=
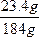 ×100%=12.72%
×100%=12.72% 
(8分)黄铜矿的主要成分X是由Cu、Fe、S三种元素组成的复盐,其中Cu、Fe两种元素的质量比为8∶7;将m g X粉末全部溶于200 mL的浓HNO3,反应后的溶液加水稀至 2.12 L时测得其pH=0;将稀释后的溶液分为两等份,向其中一份溶液中滴加浓度为6. 05 mol/L的NaOH溶液,向另一份溶液中滴加0.600 mol/L Ba(NO3)2溶液,两溶液中均生成沉淀,且沉淀的质量随所加溶液的体积变化如下图所示:
(1)请通过计算确定:m=________。
(2)X的摩尔质量为368 g/mol,则X的化学式为________________。
(3)将一定质量的Fe、Cu的混合物平均分成四等份,每份13.2 g,分别加入同浓度的稀硝酸,充分反应后,在标准状况下生成NO的体积与剩余金属的质量见下表(设硝酸的还原产物只有NO):
| 实验编号 | ① | ② | ③ | ④ |
| 稀硝酸体积/mL | 100 | 200 | 300 | 400 |
| 剩余金属质量/g | 9.0 | 4.8 | 0 | 0 |
| NO体积/L | 1.12 | 2.24 | 3.36 | V |
回答下列问题:
①写出实验①中发生反应的离子方程式___________________________________。
②实验④中V=________。
如图所示3套实验装置,分别回答下列问题。
(1)装置1为铁的吸氧腐蚀实验。一段时间后, 向插入碳棒的玻璃筒内滴入酚酞溶液,可观察到碳棒附近的溶液变红,该电极反应为 。
(2)装置2中的石墨是 极(填“正”或“负” ),该装置发生的总反应的离子方程式为 。
(3)装置3中甲烧杯盛放200 mL 0.2 mol/L的NaCl溶液,乙烧杯盛放200 mL 1.0 mol/L的CuSO4溶液。反应一段时间后,停止通电。向甲烧杯中滴入几滴酚酞溶液,观察到石墨电极附近首先变红。
|
