题目内容
10.向10mL pH=12的NaOH溶液中加入10mL某酸,再滴入几滴甲基橙,溶液呈红色,则这种酸可能是( )| A. | pH=2的硫酸 | B. | 0.01 mol•L-1的甲酸 | ||
| C. | pH=2的醋酸 | D. | 0.01 mol•L-1的硝酸 |
分析 向10mL pH=12的NaOH溶液中加入10mL某酸,再滴入几滴甲基橙,溶液呈红色,说明溶液呈酸性,反应后酸过量,以此解答该题.
解答 解:A.加入10mL pH=2的硫酸,恰好反应生成硫酸钠,溶液呈中性,故A错误;
B.加入0.01 mol•L-1的甲酸,生成甲酸钠,为强碱弱酸盐,水解呈碱性,故B错误;
C.pH=2的醋酸浓度比pH=12的NaOH溶液大,反应后醋酸过量,溶液呈酸性,故C正确;
D.加入0.01 mol•L-1的硝酸,恰好反应生成硝酸钠,溶液呈中性,故D错误;
故选C.
点评 本题考查酸碱混合的定性判断和计算,为高考常见题型,题目难度中等,侧重于学生的分析能力和计算能力的考查,注意明确酸碱物质的量的关系的确定以及电解质强弱的判断.

练习册系列答案
相关题目
20.Cu和浓H2SO4反应得到25g CuSO4•5H2O,被还原的H2SO4是( )
| A. | 9.8g | B. | 15.3g | C. | 19.6g | D. | 30.6g |
18.等电子体具有相同的原子数目和电子数目,下列属于等电子体的是 ( )
| A. | NH3和H2O | B. | NO和O2+ | C. | NO2和CO2 | D. | OH-和NH2- |
15.向质量分数为2a%,体积为10mL物质的量浓度为c1 mol•L-1的稀H2SO4中加入V mL的水,使之质量分数变为a%,此时物质的量浓度为c2 mol•L-1,则下列关系正确的是( )
| A. | V>10 2c2=c1 | B. | V<10 2c2>c1 | C. | V>10 2c2<c1 | D. | V>10 2c2>c1 |
19.[Co(NH3)4](H2O)2]3+具有几何异体构体的数目是( )
| A. | 1 | B. | 2 | C. | 3 | D. | 4 |
20.某烃的结构简式为 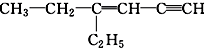 分子中饱和碳原子数为a,可能在同一直线上的碳原子数为b,可能在同一平面上的碳原子数最多为c,则a、b、c分别为( )
分子中饱和碳原子数为a,可能在同一直线上的碳原子数为b,可能在同一平面上的碳原子数最多为c,则a、b、c分别为( )
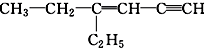 分子中饱和碳原子数为a,可能在同一直线上的碳原子数为b,可能在同一平面上的碳原子数最多为c,则a、b、c分别为( )
分子中饱和碳原子数为a,可能在同一直线上的碳原子数为b,可能在同一平面上的碳原子数最多为c,则a、b、c分别为( )| A. | 4、3、7 | B. | 4、3、8 | C. | 2、5、4 | D. | 4、6、4 |