题目内容
15.下列化学用语表达正确的是( )| A. | N2的结构式: | |
| B. | 次氯酸的结构式为:H-Cl-O | |
| C. | 硫离子的核外电子排布式:1s22s22p63s23p6 | |
| D. | NH3的电子式: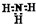 |
分析 A.用短线“-”代替共用电子对即为结构式;
B.次氯酸是共价化合物,氧原子与氢原子、氯原子分别通过1对共用电子对结合,结构式为H-O-Cl;
C.硫离子最外层为8个电子,即3p应该为6个电子;
D.NH3分子中含有3个氮氢共价键,氮原子最外层达到8电子稳定结构.
解答 解:A.N原子之间形成三对共用电子对,结构式只把共用电子对用短线表示,未成键的电子不画出.N2的结构式为N≡N,故A错误;
B.次氯酸是共价化合物,氧原子与氢原子、氯原子分别通过1对共用电子对结合,结构式为H-O-Cl,故B错误;
C.硫离子核外电子总数为18,最外层为8个电子,硫离子的核外电子排布式为1s22s22p63s23p6,故C正确;
D.NH3分子中含有3个氮氢共价键,则NH3的电子式为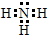 ,故D错误;
,故D错误;
故选C.
点评 本题考查了电子式、结构式、核外电子排布式的表示方法判断,题目难度中等,注意掌握常见的化学用语的概念及正确的表示方法,明确原子、阴阳离子、离子化合物与共价化合物的电子的区别.

练习册系列答案
相关题目
5.胡椒酚是植物挥发油的成分之一,它的结构简式为:HO- -CH2CH=CH2,下列叙述中正确的是( )
-CH2CH=CH2,下列叙述中正确的是( )
 -CH2CH=CH2,下列叙述中正确的是( )
-CH2CH=CH2,下列叙述中正确的是( )| A. | 1mol胡椒酚最多可与4mol溴发生反应 | |
| B. | 1mol胡椒酚最多可与4mol H2发生反应 | |
| C. | 胡椒酚中所有原子可能共平面 | |
| D. | 胡椒酚在水中的溶解度小于苯酚在水中的溶解度 |
3.下列关于硅及其化合物的说法中正确的是( )
| A. | 硅元素主要以单质、氧化物、硅酸盐的形式存在于自然界中 | |
| B. | 由于SiO2具有较强导电性所以可用于制造通讯光缆 | |
| C. | 常温下硅单质易跟氧气、氯气、硝酸、硫酸等发生反应 | |
| D. | 硅晶体的导电性介于导体、绝缘体之问,是重要半导体材料 |
10.下列化学用语的相关表述正确的是( )
| A. | H+(aq)+OH-(aq)=H2O(l)△H=-a kJ/mol,故1 mol NaOH固体与足量的稀盐酸反应,放出热量为akJ | |
| B. | 因CuSO4•5H2O(s)═CuSO4(s)+5H2O(1)△H=+b kJ/mol,故1 mol CuSO4(s)溶于足量水时,放出热量为bkJ | |
| C. | 因氢气的燃烧热为c kJ/mol,故电解水的热化学方程式为:2H2O(1)═2H2(g)+O2(g)△H=+c kJ/mol | |
| D. | 因N2(g)+3H2(g)?2NH3(g)△H=-d kJ/mol,故在某容器中投入1 mol N2与3 mol H2充分反应后,放出热量小于dkJ |
5.下列离子方程式书写正确的是( )
| A. | 向澄清石灰水中滴入少量的NaHCO3溶液:HCO3?+OH?+Ca2+═CaCO3↓+H2O | |
| B. | 用CH3COOH除水垢:CaCO3+2H+=H2O+CO2↑+Ca2+ | |
| C. | 少量SO2通入Ca(ClO)2溶液中:SO2+ClO-+H2O+Ca2+═CaSO4↓+2HClO | |
| D. | 少量的氯气通入溴化亚铁溶液中:Cl2+2Br-═Br2+2Cl- |
 .
.