题目内容
【题目】一定温度下,探究铜与稀HNO3的反应,反应过程如下:
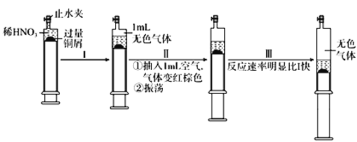
下列说法错误的是
A.过程I中生成无色气体的离子方程式是3Cu+2NO3-+8H+ =3Cu2++2NO↑+4H2O
B.步骤III反应速率比I 快的原因一定是NO2溶于水,使c(HNO3)增大
C.过程Ⅱ中气体变成红棕色的反应为2NO+O2=2NO2
D.当活塞不再移动时,再抽入空气,铜可以继续溶解
【答案】B
【解析】
铜与稀硝酸反应生成硝酸铜和一氧化氮、水,得到的无色气体是一氧化氮,抽入空气后发生反应2NO+O2=2NO2,振荡后,反应速率加快,说明二氧化氮对反应具有催化作用,据此分析。
A.过程I中生成无色气体的离子方程式为3Cu+2NO3-+8H+=3Cu2++2NO↑+4H2O,故A正确;
B.随着反应的进行,溶液里生成硝酸铜,根据氮元素守恒,溶液中c(HNO3)应比原硝酸浓度减小,不会增大,故B错误;
C.根据分析可知,过程Ⅱ中气体变成红棕色,是一氧化氮被氧化的过程,化学反应方程式为:2NO+O2=2NO2,故C正确;
D.当活塞不再移动时,再抽入空气,一氧化氮与氧气、水反应生成硝酸,能与铜继续反应,故D正确;
答案选B。

练习册系列答案
相关题目