题目内容
14.实验室为监测空气中汞蒸汽的含量;往往悬挂涂有CuI的滤纸,根据滤纸是否变色或颜色发生变化所用去的时间,来判断空气中的含汞量,其反应为:4CuI+Hg=Cu2HgI4+2Cu(1)上述反应产物Cu2HgI4中,Cu元素显+1价.
(2)以上反应中的氧化剂为CuI,当有1molCuI参与反应时,转移电子0.5mol.
(3)CuI可由Cu2+与I-直接反应制得,□Cu2++□I-→□CuI+□I3-请配平下列反应的离子方程式2Cu2++5I-═2CuI+I3-.
分析 (1)化合物中各元素化合价的代数和为0确定Cu元素化合价,该化合物中I元素显-1价、Hg元素显+2价;
(2)CuI+Hg→Cu2HgI4+2Cu中,Hg元素的化合价升高,Cu元素的化合价降低;
(3)该反应中Cu元素化合价由+2价变为+1价、I元素化合价由-1价变为-$\frac{1}{3}$价,根据转移电子相等配平方程式.
解答 解:(1)该化合物中I元素显-1价、Hg元素显+2价,化合物中各元素化合价的代数和为0,则Cu元素化合价为+1价,故答案为:+1;
(2)在反应4CuI+Hg═Cu2HgI4+2Cu中,CuI中Cu元素的化合价由+1价降为0价,CuI为氧化剂,4molCuI参加反应转移的电子为2mol,则1molCuI参与反应时,转移电子0.5mol,
故答案为:CuI;0.5;
(3)该反应中Cu元素化合价由+2价变为+1价、I元素化合价由-1价变为-$\frac{1}{3}$价,转移电子数为2,所以其方程式为2Cu2++5I-═2CuI+I3-,
故答案为:2Cu2++5I-═2CuI+I3-.
点评 本题考查氧化还原反应,为高频考点,注意从化合价的变化角度分析有关概念,从守恒的角度书写并配平离子方程式,题目难度中等.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
4.下表为元素周期表的一部分,参照元素①~⑧在表中的位置,用化学用语回答下列问题
(1)④、⑤、⑥的原子半径由大到小的顺序是Na>Al>O.
(2)②、③、⑦的最高价含氧酸的酸性由强到弱的顺序是HNO3>H2CO3>H2SiO3.
(3)①、④、⑤、⑧中的某些元素可形成既含离子键又含极性共价键的化合物,写出其中一种化合物的电子式: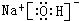 或
或 等.
等.
(4)由表中两种元素的原子按1:1组成的常见液态化合物A的稀溶液易被催化分解,可使用的催化剂为(填序号)
ab.a.MnO2 b.FeCl3 c.Na2SO3 d.KMnO4
(5)向含有酚酞的NaOH稀溶液中,逐滴滴入10%的上述A溶液,红色很快褪去.褪色原因,甲同学认为A溶液显酸性所致;乙同学认为A溶液强氧化性所致.请你设计一个简单的实验来说明甲对还是乙对.
(简易文字说明)在褪色后的溶液中再逐滴滴入NaOH溶液,若红色不恢复则说明乙对.
| 族 周期 | ⅠA | 0 | ||||||
| 1 | ① | II A | IIIA | IVA | VA | VIA | VⅡA | |
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ||||
(2)②、③、⑦的最高价含氧酸的酸性由强到弱的顺序是HNO3>H2CO3>H2SiO3.
(3)①、④、⑤、⑧中的某些元素可形成既含离子键又含极性共价键的化合物,写出其中一种化合物的电子式:
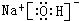 或
或 等.
等.(4)由表中两种元素的原子按1:1组成的常见液态化合物A的稀溶液易被催化分解,可使用的催化剂为(填序号)
ab.a.MnO2 b.FeCl3 c.Na2SO3 d.KMnO4
(5)向含有酚酞的NaOH稀溶液中,逐滴滴入10%的上述A溶液,红色很快褪去.褪色原因,甲同学认为A溶液显酸性所致;乙同学认为A溶液强氧化性所致.请你设计一个简单的实验来说明甲对还是乙对.
(简易文字说明)在褪色后的溶液中再逐滴滴入NaOH溶液,若红色不恢复则说明乙对.
5.下列烷烃只有两种同分异构体的是( )
| A. | 丁烷 | B. | 丙烷 | C. | 乙烷 | D. | 戊烷 |
2.表是某品牌柠檬汁饮料标签的部分内容,则该饮料中维生素C(分子式为C6H8O6)的物质的量浓度为( )
| Nutrition Facts营养成分 500mL含量 | |
| 热量 710kJ | 碳水化合物 42g |
| 蛋白质 0g | 脂肪酸 0g |
| 维生素C 100mg | |
| 中国居民膳食营养素日推荐摄入量(RNI):维生素C 100mg | |
| A. | 1.14×10-3 mol•L-1 | B. | 0.2 mg•mL-1 | ||
| C. | 1.42×10-3 mol•L-1 | D. | 0.2 mol•L-1 |
9.下列事实或性质与胶体没有直接关系的是( )
| A. | 在河流入海处易形成三角洲 | |
| B. | 用微波手术刀进行外科手术,可使开到处的血液迅速凝固,减少失血 | |
| C. | 同一钢笔使用不同牌号的墨水容易堵塞 | |
| D. | 氢氧化铁固体溶于盐酸得澄清溶液 |
6.一定条件下,等物质的量的X(g)与Y(g)在密闭容器中进行可逆反应:X(g)+Y(g)?2Z(g)+W(s)△H<0;下列叙述正确的是( )
| A. | 改变条件使平衡常数K增大,X的转化率增大 | |
| B. | 达到平衡时,反应速率2v正(X)=v逆(Z) | |
| C. | 若单位时间内消耗n mol X,同时生成n mol W,则说明该反应达到平衡状态 | |
| D. | 在该反应达到平衡时,向体系内充入惰性气体,体积增大,平衡将向右移动 |
3.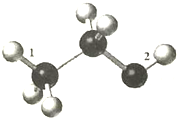 某由C、H、O组成的有机物分子结构模型如图(图中三种不同大小的球,分别表示三种不同的原子,数字“1”和“2”分别表示对应的化学键).下列有关说法正确的是( )
某由C、H、O组成的有机物分子结构模型如图(图中三种不同大小的球,分别表示三种不同的原子,数字“1”和“2”分别表示对应的化学键).下列有关说法正确的是( )
 某由C、H、O组成的有机物分子结构模型如图(图中三种不同大小的球,分别表示三种不同的原子,数字“1”和“2”分别表示对应的化学键).下列有关说法正确的是( )
某由C、H、O组成的有机物分子结构模型如图(图中三种不同大小的球,分别表示三种不同的原子,数字“1”和“2”分别表示对应的化学键).下列有关说法正确的是( )| A. | 该物质难溶于水,密度比水大 | |
| B. | 该物质不存在同分异构体 | |
| C. | 该物质与钠反应时,化学键“2”将断裂 | |
| D. | 该物质不可能发生取代反应 |
