题目内容
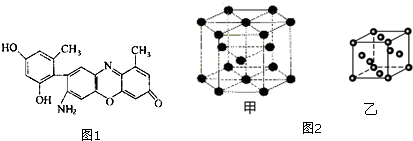
15.下列3种有机化合物A:CH2=CH2、B:CH3COOH、C: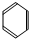
(1)化合物A、B中的官能团的名称分别是碳碳双键、羧基.
(2)能使溴的四氯化碳溶液褪色反应的化学方程式为:CH2=CH2+Br2→CH2BrCH2Br,该反应类型为:加成反应.
(3)能与乙醇发生酯化反应的化学方程式为:CH3COOH+CH3CH2OH
 CH3COOC2H5+H2O.
CH3COOC2H5+H2O.(4)
 在浓硫酸作用下,与浓硝酸反应的化学方程式为:C6H6+HNO3$→_{50℃-60℃}^{浓硫酸}$C6H5NO2+H2O.
在浓硫酸作用下,与浓硝酸反应的化学方程式为:C6H6+HNO3$→_{50℃-60℃}^{浓硫酸}$C6H5NO2+H2O.
分析 (1)根据官能团的结构可知,化合物A、B中含有的官能团为碳碳双键、羧基;
(2)加成反应:有机物分子中的不饱和键断裂,断键原子与其它原子或原子团相结合,生成新的化合物,乙烯含有碳碳不饱和键,能和溴发生加成反应;
(3)乙酸和乙醇发生酯化反应生成乙酸乙酯;
(4)苯、浓硫酸、浓硝酸在50~60℃的水浴中反应生成硝基苯.
解答 解:(1)根据官能团的结构可知,化合物A为乙烯、B为乙酸它们结构中含有的官能团为碳碳双键、羧基,
故答案为:碳碳双键、羧基;
(2)含有不饱和键的有机分子能发生加成反应,乙烯含有碳碳双键,能和溴反应生成1,2-二溴乙烷,化学方程式为Br2+CH2=CH2→BrCH2CH2Br,
故答案为:CH2=CH2+Br2→CH2BrCH2Br;加成反应;
(3)乙酸与乙醇在浓硫酸作用下加热发生酯化反应生成乙酸乙酯和水,该反应方程式为:CH3COOH+CH3CH2OH CH3COOC2H5+H2O,
CH3COOC2H5+H2O,
故答案为:CH3COOH+CH3CH2OH CH3COOC2H5+H2O;
CH3COOC2H5+H2O;
(4)苯和浓硝酸、浓硫酸在50℃~60℃发生硝化反应,硝基取代苯环上的氢原子,生成硝基苯和水,该反应为:C6H6+HNO3$→_{50℃-60℃}^{浓硫酸}$C6H5NO2+H2O,
故答案为:C6H6+HNO3$→_{50℃-60℃}^{浓硫酸}$C6H5NO2+H2O.
点评 本题以有机物的结构为载体考查官能团的结构与性质,题目难度不大,根据结构推测性质,旨在考查学生对知识的综合运用能力.

练习册系列答案
 开心蛙状元测试卷系列答案
开心蛙状元测试卷系列答案
相关题目
5.下列各组离子在溶液中能大量共存的是( )
| A. | Ca2+、K+、NO3-、Cl- | B. | Na+、Ba2+、Br-、SO32- | ||
| C. | H+、Na+、SiO32-、Cl- | D. | H+、Fe3+、I-、NO3- |
6.工业上冶炼金属铝,经常采用的方法是( )
| A. | 热氧化法 | B. | 热分解法 | C. | 电解法 | D. | 热还原法 |
3.下表是A、B、C、D、E五种有机物的有关信息:
回答下列问题:
(1)A与溴的四氯化碳溶液反应的生成物的名称是1,2-二溴乙烷.
(2)A与氢气发生加成反应后生成物质F,与F在分子组成和结构上相似的有机物有一大类(俗称“同系物”),它们均符合通式CnH2n+2.当n=4时,这类有机物开始出现同分异构体.
(3)B具有的性质是②③(填序号).
①无色无味液体 ②有毒 ③不溶于水 ④密度比水大
⑤与酸性KMnO4溶液和溴水反应褪色 ⑥任何条件下不与氢气反应
写出在浓硫酸作用下,B与浓硝酸反应的化学方程式: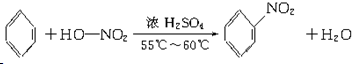 .
.
(4)据报道,最近摩托罗拉公司研制了一种由有机物C的同系物(该有机物的碳原子数比有机物C的碳原子数少1)和氧气以及强碱作电解质溶液的新型手机电池,电量可达现用镍氢电池或锂电池的10倍.该燃料电池的负极上的电极反应式为CH3OH-6e-+8OH-=CO32-+6H2O,当外电路通过1.2mol e-时,理论上消耗该有机物为6.4g.
| A | ①能使溴的四氯化碳溶液褪色;②比例模型为 ;③能与水在一定条件下反应生成C ;③能与水在一定条件下反应生成C |
| B | ①由C、H两种元素组成;②球棍模型为 |
| C | ①由C、H、O三种元素组成;②能与Na反应,但不能与NaOH溶液反应;③能与E反应生成相对分子质量为100的酯 |
| D | ①相对分子质量比C少2;②能由C氧化而成. |
| E | ①由C、H、O三种元素组成;②球棍模型为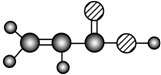 |
(1)A与溴的四氯化碳溶液反应的生成物的名称是1,2-二溴乙烷.
(2)A与氢气发生加成反应后生成物质F,与F在分子组成和结构上相似的有机物有一大类(俗称“同系物”),它们均符合通式CnH2n+2.当n=4时,这类有机物开始出现同分异构体.
(3)B具有的性质是②③(填序号).
①无色无味液体 ②有毒 ③不溶于水 ④密度比水大
⑤与酸性KMnO4溶液和溴水反应褪色 ⑥任何条件下不与氢气反应
写出在浓硫酸作用下,B与浓硝酸反应的化学方程式:
 .
.(4)据报道,最近摩托罗拉公司研制了一种由有机物C的同系物(该有机物的碳原子数比有机物C的碳原子数少1)和氧气以及强碱作电解质溶液的新型手机电池,电量可达现用镍氢电池或锂电池的10倍.该燃料电池的负极上的电极反应式为CH3OH-6e-+8OH-=CO32-+6H2O,当外电路通过1.2mol e-时,理论上消耗该有机物为6.4g.
20.为达到下列实验目的,所选试剂不足的是( )
| 选项 | 实验目的 | 选用试剂 |
| A | 探究Cl2、Br2、I2的氧化性强弱顺序 | 氯水、溴水、KI溶液 |
| B | 探究化学反应的能量变化 | Ba(OH)2•8H2O、NH4Cl晶体 |
| C | 证明海带灰中含有碘元素 | 海带灰、稀硫酸、3%的H2O2溶液、淀粉溶液 |
| D | 证明淀粉是否水解 | 淀粉溶液、稀硫酸、NaOH溶液、银氨溶液 |
| A. | A | B. | B | C. | C | D. | D |
7.高温下,炽热的铁与水蒸气在密闭容器中进行反应:3Fe(s)+4H2O(g)?Fe3O4(s)+4H2(g),下列条件的改变对其反应速率几乎无影响的是( )
| A. | 增加H2的量 | |
| B. | 将容器的体积缩小一半 | |
| C. | 压强不变,充入氮气使容器体积增大 | |
| D. | 体积不变,充入氮气使容器压强增大 |
4.据报道,一种“月球制氧机”可利用聚焦太阳能产生的高温加热月球土壤,制得氧气.据此可推测月球土壤中一定含有( )
| A. | 氧化物 | B. | 氧气 | C. | 水 | D. | 氧元素 |
5.甲基苯基甲醇(Methylphenylcarbinol)可以用作食用香精,其结构简式为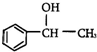 则甲基苯基甲醇的分子式为( )
则甲基苯基甲醇的分子式为( )
 则甲基苯基甲醇的分子式为( )
则甲基苯基甲醇的分子式为( )| A. | C8H10O | B. | C9H10O | C. | C8H8O | D. | C8H12O |