题目内容
【题目】秦皮是一种常用的中药,具有抗炎镇痛、抗肿瘤等作用。“秦皮素”是其含有的一种有效成分,结构简式如图所示,有关其性质叙述不正确的是( )
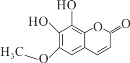
A.该有机物分子式为C10H8O5
B.分子中有四种官能团
C.该有机物能发生加成、氧化、取代等反应
D.1mol该化合物最多能与3molNaOH反应
【答案】D
【解析】
由结构可知分子式,秦皮中物质分子中含酚-OH、碳碳双键、-COOC-及醚键,结合酚、烯烃及酯的性质来解答。
A.由结构可知分子式为C10H8O5,A正确;
B.含有羟基、酯基、碳碳双键以及醚键4种官能团,B正确;
C.含苯环、碳碳双键可发生加成反应,碳碳双键、-OH可发生氧化反应,-OH、-COOC-可发生取代反应,C正确;
D.能与氢氧化钠反应的为酚羟基和酯基,且酯基可水解生成羧基和酚羟基,则1mol 该化合物最多能与4mol NaOH 反应,D错误;
故合理选项是D。

练习册系列答案
 状元坊全程突破导练测系列答案
状元坊全程突破导练测系列答案 直通贵州名校周测月考直通名校系列答案
直通贵州名校周测月考直通名校系列答案
相关题目