题目内容
8.在一个固定容积的密闭容器中,加入2molA和1molB发生反应:2A(g)+B(g)?3C(g)+D(g),达到平衡时,C的浓度为n mol•L-1.(1)若维持温度不变,按下列各种配比为起始物质,达到平衡后,C仍为n mol•L-1的是DE(填字母序号,下同)
A.4molA+2molB
B.2molA+1molB+3molC+1molD
C.3molA+1molB
D.3molC+1molD
E.1molA+0.5molB+1.5molC+0.5molD
(2)C的浓度大于n mol•L-1的是ABC.
(3)将可逆反应中A(g)改为A(s),则C的浓度仍为 n mol•L-1的是CDE.
分析 (1)反应2A(g)+B(g)?3C(g)+D(g),在恒温恒容下,不同途径达到平衡后,C的浓度仍为nmol/L,说明与原平衡为等效平衡,按化学计量数转化到方程式的左边,只要满足n(A)=2mol,n(B)=1mol即可,据此进行分析;
(2)C的浓度大于n mol•L-1,即在原平衡基础上向正反应方向移动或者反应物成倍增加,据此分析;
(3)将可逆反应中A(g)改为A(s),因为固体的量对平衡无影响,所以在恒温恒容下,不同途径达到平衡后,C的浓度仍为nmol/L,说明与原平衡为等效平衡,按化学计量数转化到方程式的左边,只要满足n(A)≥2mol,n(B)=1mol即可.
解答 解:(1)根据等效平衡,按化学计量数转化到方程式左边应该满足与初始加入的2molA和1molB相等.
A、4 mol A+2 mol B与初始物质的量2molA 和1molB不同,不属于等效平衡,故A错误;
B、2molA+1molB+3molC+1molD换算成A、B,物质的量分别为4mol、2mol,与初始量不同,不属于等效平衡,故B错误;
C、3molA+1molB与初始物质的量2molA 和1molB不同,不属于等效平衡,故C错误;
D、3 mol C+1 mol D换算成A、B,物质的量分别为2mol、1mol,与初始量相同,故D正确;
E、1molA+0.5molB+1.5molC+0.5molD换算成A、B,物质的量分别为2mol、1mol,与初始量相同,故E正确;
故选:DE;
(2)A、4 mol A+2 mol B为初始物质的量2molA 和1molB的2倍,则平衡时C的浓度大于n mol•L-1,故A正确;
B、2molA+1molB+3molC+1molD换算成A、B物质的量分别为4mol、2mol,为初始物质的量2molA 和1molB的2倍,则平衡时C的浓度大于n mol•L-1,故B正确;
C、3molA+1molB与初始物质的量2molA 和1molB相比,相对于增加A的量平衡正向移动,则平衡时C的浓度大于n mol•L-1,故C正确;
故选:ABC;
(3)将可逆反应中A(g)改为A(s),因为固体的量对平衡无影响,所以在恒温恒容下,不同途径达到平衡后,C的浓度仍为nmol/L,说明与原平衡为等效平衡,按化学计量数转化到方程式的左边,只要满足n(A)≥2mol,n(B)=1mol即可,所以根据(1)的分析,CDE正确;故选:CDE.
点评 本题考查化学平衡的有关计算、等效平衡,难度中等,构建平衡建立的途径是解题关键,注意等效平衡规律:1、恒温恒压下,按化学计量数转化到一边,满足对应物质的物质的量之比相同,为等效平衡;2、恒温恒容下,若反应前后气体气体发生变化,按化学计量数转化到一边,满足对应物质的物质的量相等,为等效平衡;若反应前后气体的体积不变,按化学计量数转化到一边,满足对应物质的物质的量之比相同,为等效平衡.

 阅读快车系列答案
阅读快车系列答案| A. |  根据图可判断:2O3(g)=3O2(g);△H=-44.8KJ/mol | |
| B. |  根据图可判断A(g)?2C(g)在使用催化剂时的反应速率大,且面积Saco>Sbdo | |
| C. | 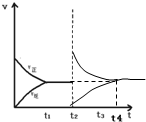 根据图可判断2A(g)?C(g)在恒温恒压时再充入A(g),t4重新达到平衡时与上一平衡为等效平衡 | |
| D. |  图表示2NO2(g)?N2O4(g)反应,当其它条件相同时,改变压强达到平衡时C(NO2)变化情况,且P1>P2 |
| A. | 氢气还原氧化铜实验中,先通氢气后加热氧化铜 | |
| B. | 不慎将酸溅到眼中,应立即用水冲洗,边洗边眨眼睛 | |
| C. | 实验结束后将所有的废液倒入下水道排出实验室,以免污染实验室 | |
| D. | 在制氧气时排水法收集氧气后出现倒吸现象,立即松开试管上的橡皮塞 |
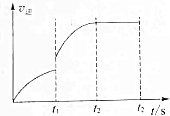 将N2,H2按物质的量比为1:3的比例混合于5L的恒容密闭容器中进行反应N2+3H2?2NH3,△H<0,若该反应的逆反应速率随时间变化的关系如图所示.则t1时改变的条件不可能是( )
将N2,H2按物质的量比为1:3的比例混合于5L的恒容密闭容器中进行反应N2+3H2?2NH3,△H<0,若该反应的逆反应速率随时间变化的关系如图所示.则t1时改变的条件不可能是( )| A. | 升温 | B. | 使用催化剂 | C. | 加入一定量NH3 | D. | 加入一定量N2 |
| 压强/MPa 体积分数/% 温度/℃ | 1.0 | 2.0 | 3.0 |
| 810 | 54.0 | a | b |
| 915 | c | 75.0 | d |
| 1000 | e | f | 85.0 |
(1)该反应的△S>(填“>”、“<”或“=”,下同)0;△H>0.
(2)表中该反应的化学平衡常数的值最大时对应的温度是1000℃;判断理由是该反应的正反应为吸热反应,升高温度平衡正向移动,平衡常数增大.
(3)在915℃、2.0MPa时X的平衡转化率为60%.
(4)用压强替代浓度得到的平衡常数叫作压强平衡常数(Kp).在810℃、1.0MPa下,Kp=0.634MPa.
(5)能同时提高X的反应速率和转化率的措施是A.
A.升高温度 B.增大压强 C.加催化剂 D分离Z.
| 选项 | 甲 | 乙 |
| A | 物质中的粒子数 | 阿伏加德罗常数 |
| B | 固体体积 | 固体密度 |
| C | 溶液中溶质的物质的量浓度 | 溶液体积 |
| D | 标准状况下气体摩尔体积 | 标准状况下气体体积 |
| A. | A | B. | B | C. | C | D. | D |
 A,B,C,D,E是原子序数依次增大的五种短周期元素,A是半径最小的元素,C是半径最大的元素.B和D分别为同主族,且D的质子数是B的2倍,A与E形成的化合物的化学式为AE,其分子中含18个电子,请回答下列问题:
A,B,C,D,E是原子序数依次增大的五种短周期元素,A是半径最小的元素,C是半径最大的元素.B和D分别为同主族,且D的质子数是B的2倍,A与E形成的化合物的化学式为AE,其分子中含18个电子,请回答下列问题: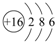 .
.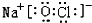 ,这种化合物中所含的化学键类型有离子键、共价键.
,这种化合物中所含的化学键类型有离子键、共价键.