题目内容
将0.8g NaOH和1.06g Na2CO3混合并配成溶液,向溶液中滴加0.1 mol·L-1稀盐酸。下列图像能正确表示加入盐酸的体积和生成CO2的物质的量的关系的是 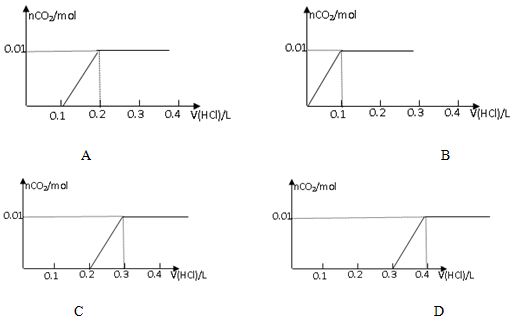

D
试题分析:氢氧化钠和碳酸钠的物质的量分别是0.02mol和0.01mol。加入盐酸时,首先和氢氧化钠反应,然后再和碳酸钠反应。由于碳酸钠和盐酸的反应是分步进行的,首先生成碳酸氢钠,最后再和碳酸氢钠反应生成CO2气体,有关反应的方程式是NaOH+HCl=NaCl+H2O、Na2CO3+HCl=NaHCO3+NaCl、NaHCO3+HCl=NaCl+H2O+CO2↑。所以氢氧化钠和碳酸钠的物质的量可知,图像正确的应该是选项D,答案选D。
点评:该题的属于中等浓度的试题。关键是搞清楚反应的先后顺序,特别是碳酸钠和盐酸反应的分步进行,尤为重要。

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
