题目内容
下列说法中,正确的是
A 1 mol 氢 B 1. 5mol H2O
C 2 mol 铁钉 D 3 mol 西瓜
B
解析试题分析:mol表示微观粒子,B项符合;C、D选项是宏观物质,不适合;A选项氢含义不明确,mol后紧跟微粒符号。
考点:本题考察mol单位的使用。

练习册系列答案
相关题目
过氧化钠与CO2作用,反应的化学方程式为2Na2O2+2CO2=2Na2CO3+O2↑。当0.2molNa2O2与足量CO2完全反应后,下表对生成物Na2CO3和O2的描述中正确的是
| | Na2CO3的质量 | 关于O2的描述 |
| A | 21.2g | O2的摩尔质量是36g·mol-1 |
| B | 21.6g | 生成标准状况下O2的体积为2.24L |
| C | 21.6g | O2的摩尔质量是34g·mol-1 |
| D | 22.4 g | 生成标准状况下O2的体积为2.24mL |
amolFe与一定量的硝酸在一定条件下充分反应,将生成的气体与标准状况下b g O2混合,恰好能被水完全吸收,则a和b的关系可能是
| A.0.5a≤b≤0.75a | B.16a≤b≤24a | C.0.2a≤b≤0.3a | D.无法确定 |
NO、NO2、O2按照一定比例通入水中,能被完全吸收,无剩余气体,若NO、NO2、O2的气体体积分别为a、b、 c、则a:b:c可能为( )
| A.1:5:2 | B.2:5:1 | C.5:1:2 | D.5:2:1 |
设NA为阿伏加德罗常数的值,下列说法中正确的是
| A.标准状况下,2.24L乙炔中含σ键数目为0.1 NA |
| B.常温常压下,1.6gO2所含氧原子数目为0.1NA |
| C.5.6gFe和足量稀硝酸反应,转移电子数目为0.2NA |
| D.1L0.1mol·L—1Na2CO3溶液中含阴、阳离子总数目为0.3NA |
用NA表示阿伏加德罗常数的值,下列叙述正确的是
| A.24g NaH中阴离子所含电子总数为NA |
| B.标准状况下,22.4 L苯中含有C—H键数目为6NA |
| C.在碳酸钠溶液中,若c(CO32-)="1" mol?L-1,则c(Na+)="2" mol?L-1 |
| D.通过MnO2催化使H2O2分解,产生32gO2时转移电子数为2NA |
有一稀硫酸和稀硝酸的混合酸,其中H2SO4和HNO3的物质的量浓度分别是4mol/L和2mol/L,取10mL此混合酸,向其中加入过量的铁粉,待反应结束后,可产生标准状况下气体的体积为(设反应中HNO3被还原成NO)( )
| A.0.448L | B.0.672L | C.0.896L | D.0.224L |
向100mLBaCl2、AlCl3和FeCl3的混合溶液A中,逐滴加入Na2SO4和NaOH的混合溶液B,产生的沉淀总物质的量和加入溶液B的体积关系如图所示: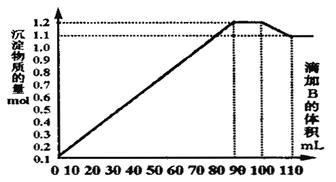
(1)当加入B溶液110 mL时,溶液中的沉淀是 (填化学式)
(2)将A.B溶液中各溶质的物质的量浓度填入下表:
| 溶 质 | Na2SO4 | BaCl2 | AlCl3 | FeCl3 |
| /mol·L-1 | | | | |
(3)写出滴加B溶液90-100mL时的离子方程式:
。
下列化学表述正确的是
A.氯化钠的晶体模型: |
B.铍原子最外层的电子云图: |
| C.次氯酸的结构式:H-O-Cl |
| D.CH3CHOHCH(CH3)2名称:2-3-二甲基丙醇 |