题目内容
(2012?江苏)[物质结构与性质]
一项科学研究成果表明,铜锰氧化物(CuMn2O4)能在常温下催化氧化空气中的一氧化碳和甲醛(HCHO).
(1)向一定物质的量浓度的Cu(NO3)2 和Mn(NO3)2 溶液中加入Na2CO3 溶液,所得沉淀经高温灼烧,可制得CuMn2O4.
①Mn2+基态的电子排布式可表示为
②NO3-的空间构型是
(2)在铜锰氧化物的催化下,CO 被氧化为CO2,HCHO 被氧化为CO2 和H2O.
①根据等电子体原理,CO 分子的结构式为
②H2O 分子中O 原子轨道的杂化类型为
③1mol CO2 中含有的σ键数目为
(3)向CuSO4 溶液中加入过量NaOH 溶液可生成[Cu (OH)4]2-.不考虑空间构型,[Cu(OH)4]2-的结构可用示意图表示为
 .
.
一项科学研究成果表明,铜锰氧化物(CuMn2O4)能在常温下催化氧化空气中的一氧化碳和甲醛(HCHO).
(1)向一定物质的量浓度的Cu(NO3)2 和Mn(NO3)2 溶液中加入Na2CO3 溶液,所得沉淀经高温灼烧,可制得CuMn2O4.
①Mn2+基态的电子排布式可表示为
1s22s22p63s23p63d5(或[Ar]3d5)
1s22s22p63s23p63d5(或[Ar]3d5)
.②NO3-的空间构型是
平面三角形
平面三角形
(用文字描述).(2)在铜锰氧化物的催化下,CO 被氧化为CO2,HCHO 被氧化为CO2 和H2O.
①根据等电子体原理,CO 分子的结构式为
C≡O
C≡O
.②H2O 分子中O 原子轨道的杂化类型为
sp3
sp3
.③1mol CO2 中含有的σ键数目为
2×6.02×1023个(或2mol)
2×6.02×1023个(或2mol)
.(3)向CuSO4 溶液中加入过量NaOH 溶液可生成[Cu (OH)4]2-.不考虑空间构型,[Cu(OH)4]2-的结构可用示意图表示为


分析:(1)①Mn的原子序数为25,根据能量最低原理可写出Mn的基态原子的电子排布式,进而可确定Mn2+基态的电子排布式;
②利用加成电子对互斥模型判断;
(2)①根据N2与CO为等电子体,结合等电子体结构相似判断;
②根据中心原子形成的δ键和孤电子对数判断杂化类型;
③据CO2的结构式O=C=O判断;
(3)[Cu(OH)4]2-中与Cu2+与4个OH-形成配位键.
②利用加成电子对互斥模型判断;
(2)①根据N2与CO为等电子体,结合等电子体结构相似判断;
②根据中心原子形成的δ键和孤电子对数判断杂化类型;
③据CO2的结构式O=C=O判断;
(3)[Cu(OH)4]2-中与Cu2+与4个OH-形成配位键.
解答:解:(1)①Mn的原子序数为25,基态原子的电子排布式为,1s22s22p63s23p63d54s2,则Mn2+基态的电子排布式可表示为1s22s22p63s23p63d5(或[Ar]3d5),故答案为:1s22s22p63s23p63d5(或[Ar]3d5);
②NO3-中N原子形成3个δ键,没有孤电子对,则应为平面三角形,故答案为:平面三角形;
(2)①N2与CO为等电子体,二者结构相似,N2的结构为N≡N,则CO的结构为C≡O,故答案为:C≡O;
②H2O 分子中O形成2个δ键,孤电子对数为
=2,则为杂化sp3;
③CO2的结构式为O=C=O,分子中C形成2个δ键,则1molCO2中含有的σ键数目为×6.02×1023个(或2mol),
故答案为:2×6.02×1023个(或2mol);
(3))[Cu(OH)4]2-中与Cu2+与4个OH-形成配位键,可表示为 ,
,
故答案为: .
.
②NO3-中N原子形成3个δ键,没有孤电子对,则应为平面三角形,故答案为:平面三角形;
(2)①N2与CO为等电子体,二者结构相似,N2的结构为N≡N,则CO的结构为C≡O,故答案为:C≡O;
②H2O 分子中O形成2个δ键,孤电子对数为
| 6-2×1 |
| 2 |
③CO2的结构式为O=C=O,分子中C形成2个δ键,则1molCO2中含有的σ键数目为×6.02×1023个(或2mol),
故答案为:2×6.02×1023个(或2mol);
(3))[Cu(OH)4]2-中与Cu2+与4个OH-形成配位键,可表示为
 ,
,故答案为:
 .
.点评:本题综合考查物质的结构与性质知识,侧重于电子排布式、等电子体、杂化类型与配位键等知识,题目难度中等,注意把握杂化类型的判断方法.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
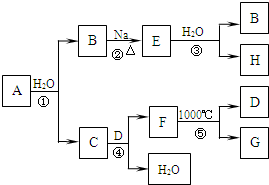 (2012?江苏一模)某ⅡA族元素是自然界存在最广泛的元素,常以化合物F存在,从其单质A起始发生的一系列化学反应如图所示.下列说法正确的是( )
(2012?江苏一模)某ⅡA族元素是自然界存在最广泛的元素,常以化合物F存在,从其单质A起始发生的一系列化学反应如图所示.下列说法正确的是( ) (2012?江苏一模)亮菌甲素为利胆解痉药适用于急性胆囊炎治疗等,其结构简式如图.下列有关叙述正确的是( )
(2012?江苏一模)亮菌甲素为利胆解痉药适用于急性胆囊炎治疗等,其结构简式如图.下列有关叙述正确的是( )