题目内容
【题目】开发新型储氢材料是氢能源利用的重要研究方向之一。请回答以下问题:
(1)Ti(BH4)3是一种储氢材料,可由TiCl4和LiBH4反应制得。
①基态Ti3+的电子排布式为____________________;LiBH4中Li、B、H元素的电负性由大到小的排列顺序为_________________。
②另有一种含钛元素的新型材料,其理论结构模型如图所示,图中虚线框内碳原子的杂化轨道类型为____________。

(2)氨硼烷(NH3BH3)是优良的储氢材料,少量氨硼烷可以由硼烷(B2H6)和NH3合成。
①NH3BH3中是否存在配位键__________(填“是”或“否”);与NH3BH3互为等电子体的分子的化学式为__________。
②B、C、N与O元素的第一电离能由大到小的顺序为___________________。
③氨硼烷在高温下释放氢后生成的立方氮化硼晶体,具有类似金刚石的结构,硬度略小于金刚石。则立方氮化硼晶体可用作___________(选填下列字母序号)。
a.切削工具 b.钻探钻头 c.导电材料 d.耐磨材料
(3)一种有储氢功能的铜合金晶体具有面心立方最密堆积的结构,晶胞中Cu原子处于面心,Au原子处于顶点位置,氢原子可进入到由Cu原子与Au原子构成的四面体空隙中。
①若将Cu原子与Au原子等同看待,该晶体储氢后的晶胞结构与CaF2的结构相似,该晶体储氢后的化学式为________________;
②铜与其它许多金属及其化合物都可以发生焰色反应,其原因是_______________。
(4)金属氢化物也是具有良好发展前景的储氢材料。某储氢材料是短周期金属元素R的氢化物。R的部分电离能如下表所示:
I1/KJ·mol-1 | I2/KJ·mol-1 | I3/KJ·mol-1 | I4/KJ·mol-1 | I5/KJ·mol-1 |
738 | 1451 | 7733 | 10540 | 13630 |
①该金属元素是___________(填元素符号)..
②若氢化物的晶胞结构如图所示(有4个H原子位于面上,其余H原子位于晶胞内),已知该晶体的密度为ρg·cm-3,则该晶胞的体积为__________cm3[用含ρ、NA的代数式表示(其中NA为阿伏加德罗常数的值)]。

【答案】 1s22s22p63s23p63d1 H>B>Li sp、sp2、sp3 是 C2H6 N>O>C>B a b d Cu3AuH8 激发态的电子从能量较高的轨道跃迁到能量较低的轨道时,以一定波长的光的形式释放能量 Mg ![]()
【解析】(1)①Ti是第22号元素,原子的核外电子排布为1s22s22p63s23p63d24s2,转化为Ti3+应该失去3个电子,离子的电子排布为1s22s22p63s23p63d1。Li为金属一定是电负性较小,H是非金属中电负性较小的元素,所以电负性顺序为:H>B>Li。
②虚线框中碳原子有形成单键(连接四个碳原子)、双键(连接三个碳原子)和三键(连接两个碳原子)的三种不同形态,所以杂化类型分别为sp3杂化、sp2杂化和sp杂化。可以参考下图: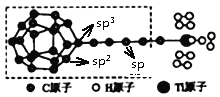 。
。
(2)①NH3中的N原子存在孤电子对,BH3中的B原子有空轨道,所以存在如下的配位键:H3N→BH3。NH3BH3与C2H6原子数相等,价电子数也相同,所以是等电子体。
②同周期元素的第一电离能应该是从左向右依次增大,但是N的p能级上有3个电子,是半满的稳定结构,所以N的第一电离能较大,得到第一电离能的顺序为:N>O>C>B。
③立方氮化硼晶体具有很高的硬度(只是略小于金刚石),所以其可以用作切削工具、钻探探头、耐磨材料等,但是和金刚石一样,该晶体应该不导电,所以不能用作导电材料。答案为abd。
(3)①氟化钙的晶胞结构为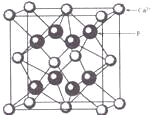 ,白球为Ca2+占据晶胞的顶点和面心,黑球为F-占据晶胞的8个四面体空隙。所以储氢晶体的晶胞中Au位于晶胞的8个顶点为8×
,白球为Ca2+占据晶胞的顶点和面心,黑球为F-占据晶胞的8个四面体空隙。所以储氢晶体的晶胞中Au位于晶胞的8个顶点为8×![]() = 1个;Cu位于晶胞的6个面心为6×
= 1个;Cu位于晶胞的6个面心为6×![]() = 3个;H占据晶胞内部的8个四面体空隙,所以有8个,晶体化学式为Cu3AuH8。
= 3个;H占据晶胞内部的8个四面体空隙,所以有8个,晶体化学式为Cu3AuH8。
②金属元素发生焰色反应的原理是:灼烧时,金属元素吸收能量,电子跃迁到激发态,激发态的电子再回落到基态,即从高能量轨道回落到低能量轨道,对外释放能量,该能量以一定波长的光的形式对外放出,就产生的焰色反应的结果。
(4)①根据该金属元素的电离能数据,因为第三电离能远大于第二电离能,说明金属元素的最外层有2个电子,元素为短周期元素,所以是Mg(Be只有4个电子,不存在I5)。
②晶胞中Mg占据顶点和体心,所以有8×![]() + 1×1=2个,H原子有4个在面上,有两个在晶胞内,所以H有4×
+ 1×1=2个,H原子有4个在面上,有两个在晶胞内,所以H有4×![]() + 2×1 = 4个,得到一个晶胞有2个Mg和4个H,一个晶胞的质量为
+ 2×1 = 4个,得到一个晶胞有2个Mg和4个H,一个晶胞的质量为![]() g。所以晶胞的体积为
g。所以晶胞的体积为![]() cm3。
cm3。

 阅读快车系列答案
阅读快车系列答案
