��Ŀ����
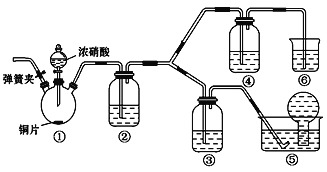
����Ŀ���ḻ��ʵ���ɫ�仯�����˻�ѧʵ��������������йط�Ӧ��ɫ�仯�������У���ȷ����
��������ˮ���ú��dz����ɫ��ʧ
�ڵ�����Һ�����ʵ����ɫ
�������м���Ũ����������ɫ
��SO2ͨ��Ʒ����Һ�С���ɫ��ȥ
�ݰ���ͨ���̪��Һ�С���ɫ
����ϡ�����ữFe(NO3)2�����
��Ũ����Ϳ����ɫʯ����ֽ�����
��Fe(OH)3����ͨ��һ��ʱ�������������ɫ����
A���٢ڢۢܢ� B���ڢۢܢݢ� C���٢ڢܢݢ� D���٢ۢܢߢ�
���𰸡�C
��������
��������������Ƶ���ˮ�д���Cl2��H2O![]() H����Cl����HClO���������ֽ⣬�����ʱ������ֽ⣬ƽ�������ƶ�����ˮ��ɫ����ȷ���ڵ�����Һ�����ʵ�����ɫ�ǵⵥ�ʵ��������ʣ������ڵⵥ�ʵļ��飬��ȷ����Ũ�����ʹ������ˮ�����DZ�ڣ����ܶ����������Ư���ԣ���ʹƷ����ɫ����ȷ���ݰ�����ˮ��Ӧ����һˮ�ϰ���һˮ�ϰ������笠����Ӻ����������ӣ�ʹˮ��Һ�ʼ��ԣ��ʿ�ʹ��̪��Һ��죬��ȷ���������ᣬ������H+��H+��ԭ����NO3 -������HNO3������ǿ�������ԣ��ܽ�ԭ����Fe2+����ΪFe3+����Һ��ƣ���ȷ������ɫ��ʯ����Һ�����죬֮��Ũ���������������ɫ������Fe(OH)3�������Ӵ�����ɣ��ڵ糡�����·�����Ӿ��������ɵĽ�����ɽ϶�������ƶ�������������ɫ������ɼ��йط�Ӧ��ɫ�仯�������У���ȷ���Ǣ٢ڢܢݢޣ�ѡ��C��ȷ��
H����Cl����HClO���������ֽ⣬�����ʱ������ֽ⣬ƽ�������ƶ�����ˮ��ɫ����ȷ���ڵ�����Һ�����ʵ�����ɫ�ǵⵥ�ʵ��������ʣ������ڵⵥ�ʵļ��飬��ȷ����Ũ�����ʹ������ˮ�����DZ�ڣ����ܶ����������Ư���ԣ���ʹƷ����ɫ����ȷ���ݰ�����ˮ��Ӧ����һˮ�ϰ���һˮ�ϰ������笠����Ӻ����������ӣ�ʹˮ��Һ�ʼ��ԣ��ʿ�ʹ��̪��Һ��죬��ȷ���������ᣬ������H+��H+��ԭ����NO3 -������HNO3������ǿ�������ԣ��ܽ�ԭ����Fe2+����ΪFe3+����Һ��ƣ���ȷ������ɫ��ʯ����Һ�����죬֮��Ũ���������������ɫ������Fe(OH)3�������Ӵ�����ɣ��ڵ糡�����·�����Ӿ��������ɵĽ�����ɽ϶�������ƶ�������������ɫ������ɼ��йط�Ӧ��ɫ�仯�������У���ȷ���Ǣ٢ڢܢݢޣ�ѡ��C��ȷ��

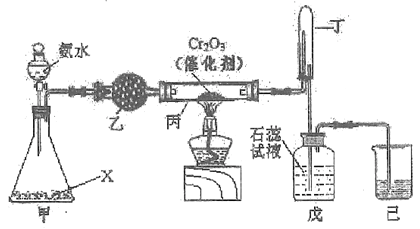
����Ŀ������һƿ�����Ǽ��ҵĻ����,��֪���ҵ�ijЩ�������±���ʾ:
���� | �۵�/�� | �е�/�� | �ܶ�g/cm3 | ˮ���ܽ��� |
�� | -98 | 57.7 | 0.93 | ���� |
�� | -84 | 77 | 0.90 | ���� |
�ݴ�,�����������ıȽϺõķ�����(����)
A. ���� B. ���� C. ��Һ�� D. ��ȡ��