题目内容
【题目】月球含有H、He、N、Na、Mg、Si等元素,是人类未来的资源宝库。
(1)3He是高效能原料,其原子核内的中子数为________________
(2)Na的原子结构示意图为____________________,Na的熔点比K的熔点__________(填“高”或“低”)
(3)MgCl2在工业上应用广泛,可由MgO制备。
①月球上某矿石经处理得到的MgO中含有少量SiO2,除去SiO2的离子方程式为______________________________。
②MgO与碳粉和氯气在一定条件下反应可制备MgCl2。若尾气可用足量NaOH溶液完全吸收,则生成的盐为________________________________(写化学式)。制备MgCl2 的化学方程式为
__________________________________________________________________。
③月壤中含有丰富的3He,从月壤中提炼100g 3He,同时可得600kg H2和70kg N2,若以得到的H2和N2为原料经一系列反应最多可生产碳酸氢铵____________kg。
【答案】 1 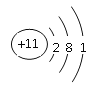 高 SiO2+2OH-=SiO32-+H2O NaCl,NaClO,Na2CO3 2MgO+C+2Cl2=2MgCl2+CO2 395
高 SiO2+2OH-=SiO32-+H2O NaCl,NaClO,Na2CO3 2MgO+C+2Cl2=2MgCl2+CO2 395
【解析】(1)3He是高效能原料,其原子核内的中子数=质量数-质子数=3-2=1;故答案为:1;
(2)钠原子时11号元素,依据核外电子排布规律写出原子结构示意图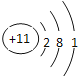 ,碱金属元素的单质,从上到下,熔点逐渐降低,Na的熔点比K的熔点高;故答案为:
,碱金属元素的单质,从上到下,熔点逐渐降低,Na的熔点比K的熔点高;故答案为: ,高;
,高;
(3)①氧化镁是碱性氧化物,二氧化硅酸式酸性氧化物,可以利用二氧化硅溶于氢氧化钠溶液除去,反应的离子方程式为:SiO2+2OH-=SiO32-+H2O;故答案为:SiO2+2OH-=SiO32-+H2O;
②MgO与碳粉和氯气在一定条件下反应可制备MgCl2,反应产物为二氧化碳,若尾气可用足量NaOH溶液完全吸收是氯气、二氧化碳和氢氧化钠反应的产物,反应的化学方程式为:CO2+2NaOH=Na2CO3+H2O,Cl2+2NaOH=NaCl+NaClO+H2O,产物为NaCl,NaClO,Na2CO3 ;MgO与碳粉和氯气在一定条件下反应可制备MgCl2,反应的化学方程式为2MgO+C+2Cl2=2MgCl2+CO2,故答案为:NaCl,NaClO,Na2CO3 ;2MgO+C+2Cl2=2MgCl2+CO2;
③得600kgH2和70kgN2,依据化学方程式N2+3H2=2NH3,若以得到H2和N2为原料想可知氢气过量,依据氮气中氮元素守恒计算,经一系列反应最多可生产碳酸氢铵的质量=![]() ×2×79g/mol=395kg;故答案为:395。
×2×79g/mol=395kg;故答案为:395。

 阅读快车系列答案
阅读快车系列答案