题目内容
【题目】用稀盐酸与稀NaOH溶液在如图所示的装置中进行中和反应。通过测定反应过程中所放出的热量可计算中和热。回答下列问题:

(1)该图中有两处未画出,它们是烧杯上方的泡沫塑料盖和。泡沫塑料的作用是。
(2)若NaOH溶液用相同浓度和体积的下列溶液代替,则对中和热数值测定结果将如何影响(填“偏大”、“偏小”、“无影响”):KOH溶液;氨水(NH3·H2O)。
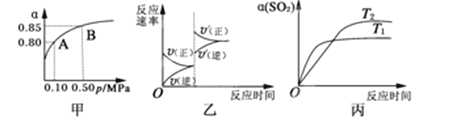
(3)某研究小组将V1mL1.0mol/LHCl溶液和V2mL未知浓度的NaOH溶液混合均匀后测量并记录溶液温度,实验结果如下图所示(实验中始终保持V1+V2=50mL)。由题干及图形可知,V1∶V2=时,酸碱恰好完全中和,此反应所用NaOH溶液的浓度应为mol/L。
【答案】
(1)环形玻璃搅拌棒减少热量的损失(合理就给分)
(2)无影响;偏小;
(3)3∶2;1.5
【解析】
试题分析:(1)由量热计的构造可知该装置的缺少仪器是环形玻璃搅拌棒;中和热测定实验成败的关键是保温工作,大小烧杯之间填满泡沫塑料的作用是减少实验过程中的热量损失;故答案为:环形玻璃搅拌棒;减少实验过程中的热量损失;
(2)若NaOH溶液用相同体积的KOH溶液代替,符合中和热的概念,中和热数值不变;氨水(NH3·H2O)为弱碱,电离过程为吸热过程,所以用氨水(NH3·H2O)代替NaOH,反应放出的热量偏小,导致中和热的数值会偏小;故答案为:无影响;偏小;
(3)当酸碱恰好反应时,放出的热量最高,从图示可知V1=30mL,V2=50mL-30mL=20mL,二者体积比为:![]() =
=![]() =
=![]() ,c(NaOH)=
,c(NaOH)=![]() =
=![]() =1.5mol/L.故答案为:
=1.5mol/L.故答案为:![]() ;1.5。
;1.5。

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目