题目内容
向盛有硝酸银水溶液的试管里加入氨水,首先形成难溶物,继续添加氨水,难溶物溶解得到无色的透明溶液,下列对此现象的说法正确的是( )
| A、反应前后Ag+的浓度不变 |
| B、沉淀溶解后,生成[Ag(NH3)2]OH难电离 |
| C、配合离子[Ag(NH3)2]+ 存在离子键和共价键 |
| D、配合离子[Ag(NH3)2]+中,Ag+提供空轨道,NH3给出孤对电子 |
考点:配合物的成键情况
专题:化学键与晶体结构
分析:A.最终得到无色的透明溶液为[Ag(NH3)2]+,所以反应后Ag+的浓度减小;
B.[Ag(NH3)2]OH为强电解质,易电离;
C.在配合离子[Ag(NH3)2]+ 中,没有离子键,仅有共价键;
D.配合物中,配位体提供孤电子对,中心原子提供空轨道形成配位键.
B.[Ag(NH3)2]OH为强电解质,易电离;
C.在配合离子[Ag(NH3)2]+ 中,没有离子键,仅有共价键;
D.配合物中,配位体提供孤电子对,中心原子提供空轨道形成配位键.
解答:
解:氨水呈碱性,向盛有硝酸银水溶液的试管里加入氨水,首先形成难溶物,Ag++OH-=AgOH↓,继续添加氨水,难溶物溶解得到无色的透明溶液,发生:AgOH+2NH3=[Ag(NH3)2]++OH-.
A.反应后形成[Ag(NH3)2]+络离子,该离子较稳定难电离,所以Ag+的浓度减小,故A错误;
B.[Ag(NH3)2]OH为强电解质,完全电离[Ag(NH3)2]OH=[Ag(NH3)2]++OH-,故B错误;
C.在配合离子[Ag(NH3)2]+ 中,Ag+提供空轨道,NH3提供孤电子对,形成的配位键,存在N、H间共价键,配位键属于特殊共价键,没有离子键,故C错误;
D.在配合离子[Ag(NH3)2]+ 中,Ag+提供空轨道,NH3提供孤电子对,形成配位键,故D正确;
故选D.
A.反应后形成[Ag(NH3)2]+络离子,该离子较稳定难电离,所以Ag+的浓度减小,故A错误;
B.[Ag(NH3)2]OH为强电解质,完全电离[Ag(NH3)2]OH=[Ag(NH3)2]++OH-,故B错误;
C.在配合离子[Ag(NH3)2]+ 中,Ag+提供空轨道,NH3提供孤电子对,形成的配位键,存在N、H间共价键,配位键属于特殊共价键,没有离子键,故C错误;
D.在配合离子[Ag(NH3)2]+ 中,Ag+提供空轨道,NH3提供孤电子对,形成配位键,故D正确;
故选D.
点评:本题考查了配合物、配位键的形成等性质,题目难度中等,明确形成配合物的条件是:有提供空轨道的中心原子,有提供孤电子对的配位体.注意[Ag(NH3)2]+ 中,没有离子键.

练习册系列答案
 天天向上口算本系列答案
天天向上口算本系列答案
相关题目
下列说法中,正确的是( )
| A、1mol H2SO4与1mol Ba(OH)2完全中和所放出的热量为中和热 |
| B、能表示氢气燃烧热的热化学方程式是2H2(g)+O2(g)═2H2O(l)△H=-571.6 kJ?mol-1 |
| C、在101kPa时,1mol碳燃烧所放出的热量一定叫碳的燃烧热 |
| D、CO燃烧是放热反应 |
1mol下列物质完全燃烧时,消耗O2的量最大的一组是( )
| A、C2H6 |
| B、C2H5OH |
| C、C2H4 |
| D、CH3COOH |
下列反应中,属于加成反应的是( )
| A、甲烷与氯气反应制取一氯甲烷 |
| B、乙酸与乙醇反应制取乙酸乙酯 |
| C、苯酚与饱和溴水反应生成三溴苯酚 |
| D、乙烯与氯化氢反应制取氯乙烷 |
下列各组物质相互混合反应后,最终有白色沉淀生成的是( )
①金属钠投入到FeCl3溶液中
②过量Ba(OH)2溶液和明矾溶液混合
③少量Ca(OH)2投入过量NaHCO3溶液中
④向NaAlO2溶液中通入过量CO2
⑤向饱和Na2CO3溶液中通入足量CO2.
①金属钠投入到FeCl3溶液中
②过量Ba(OH)2溶液和明矾溶液混合
③少量Ca(OH)2投入过量NaHCO3溶液中
④向NaAlO2溶液中通入过量CO2
⑤向饱和Na2CO3溶液中通入足量CO2.
| A、只有②③④⑤ | B、只有①②⑤ |
| C、只有②③⑤ | D、全部 |
以下作用不能使蛋白质变性的是( )
| A、加硫酸铵溶液或硫酸钠溶液 |
| B、加热 |
| C、加酸、碱或重金属盐 |
| D、紫外线照射 |
下列物质中,互为同分异构体的是( )
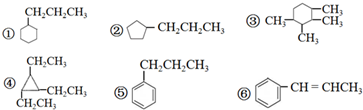

| A、①② | B、①⑤ | C、①④ | D、①③④ |
 下列是几种不同类型的漏斗,用途有差异.
下列是几种不同类型的漏斗,用途有差异.