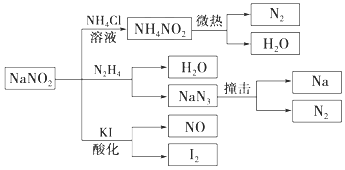
��Ŀ����
����Ŀ��N4�ķ��ӽṹ���ư����ӣ����Ľṹ��ͼ��ʾ����֪����1mol N��N����Ҫ����167kJ����������1mol N��N����ų�942kJ����������������Ϣ�����ݣ�����˵������ȷ���ǣ� �� 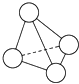
A.1 mol N4����ת��ΪN2���ų�775 kJ����
B.1 mol N4����ת��ΪN2���ų�882 kJ����
C.1 mol N4����ת��ΪN2������775 kJ����
D.1 mol N4����ת��ΪN2������882 kJ����
���𰸡�B
���������⣺����N4�ķ��ӽṹ��1molN4�����к���6molN��N����������2molN2 �� �γ�2molN��N������1moN4����ת��ΪN2��ѧ�����Ѷ������յ�����Ϊ6��167KJ=1002KJ���γɻ�ѧ���ų�������Ϊ2��942kJ=1884KJ�����Է�Ӧ���ȣ��ų�������Ϊ1884KJ��1002KJ=882KJ����ӦΪ�ų�882KJ��������B��ȷ����ѡ��B��
�����㾫����ͨ��������÷�Ӧ�Ⱥ��ʱ䣬�����ڻ�ѧ��Ӧ�зų������յ�������ͨ���з�Ӧ�ȼ����Խ����⣮

 ��Ȥ������ҵ���ϿƼ�������ϵ�д�
��Ȥ������ҵ���ϿƼ�������ϵ�д�����Ŀ���ɼ������ӻ�������ɵĻ����������������е������֣�K+��Cl����NH4+��Mg2+��CO32����Ba2+��SO42�� �� ���û��������ˮ��ó�����Һ����ȡ3��100mL����Һ�ֱ��������ʵ�飺
ʵ����� | ʵ������ | ʵ���� |
1 | ��AgNO3��Һ | �а�ɫ�������� |
2 | ������NaOH��Һ������ | �ռ�������1.12L��������ɱ�״���µ������ |
3 | ������BaCl2��Һ����Ӧ����У� ������ ���������������������м�����ϡ���ᣬȻ�������� | ��һ�γ�������Ϊ6.27g���ڶ��γ�������Ϊ2.33g |
�Իش��������⣺
��1������ʵ��1��3�жϻ������һ�������ڵ���������
��2��д��ʵ��3�еĿո�ʵ�������
��3������ʵ���Cl���Ƿ���ڵ��ж������һ�����ڡ�����һ�������ڡ�����ȷ��������
��4����Һ��K+�Ƿ���ڣ����һ�����ڡ�����һ�������ڡ�����ȷ������������һ�����ڡ�����K+���ʵ���Ũ�ȵķ�Χ������һ�������ڡ�����ȷ��������˿գ���
����Ŀ��ʵ���������������廯�ơ�����Ϊԭ���Ʊ����嶡��ķ�Ӧ���£�
NaBr+H2SO4�THBr+NaHSO4
CH3CH2CH2CH2OH+HBr ![]() CH3CH2CH2CH2Br+H2O
CH3CH2CH2CH2Br+H2O
��Բ����ƿ�м���ԭ�ϣ��������뼸����ʯ����װװ�â��������ڣ���ӦԼ40min������ӦҺ��ȴ��װΪװ�â������ֲ�Ʒ���������������б����£�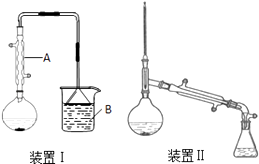
���� | ������ | ���嶡�� |
�е�/�� | 117.2 | 101.6 |
�۵�/�� | ��89.12 | ��112.4 |
�ܶ�/gcm��3 | 0.8098 | 1.2758 |
�ܽ��� | ����ˮ������Ũ���� | ������ˮ��Ũ���� |
�����ôֲ�Ʒ�����Һ©���У�����10mLˮϴ�ӣ���ȥ��ˮ�������ʣ�Ȼ��������5mLŨ���ᡢ10mLˮ��10mL����NaHCO3��Һ��10mLˮϴ�ӣ�������л��㣬������ˮ�Ȼ��ƹ��壬����1h�����˳�ȥ�Ȼ��ƣ��ٳ�ѹ�����ռ�99��103����֣�
�ش��������⣺
��1������A�������� �� ��ȴˮ��A������ϡ����¡�����ͨ�룮
��2����Բ����ƿ�м����ԭ���У���10mlˮ����7.5ml����������10g�廯�ƣ���12mLŨ���ᣮ�������ʵļ���˳���������������ȷ�𰸱�ţ���
a���٢ܢڢ�b���ܢ٢ڢ�c���ۢܢ٢�
��3���ձ�B��ʢ��NaOH��Һ�����յ�β����Ҫ�����ѧʽ������ʵ��ʹ�õ������м��ȣ��ܹ�ʹ�����Σ�
��4����Ũ����ϴ�Ӵֲ�Ʒʱ���л���ӷ�Һ©������Ͽڵ��������¿ڷų����������һ��ˮϴ��Ҫ��ϴ��
��5���Ʊ����嶡��ʱ����ֱ����װ�â�߷�Ӧ�����������ԭ���� ��
��6����ʵ��õ����嶡��6.5g������Ϊ��ֻ��ʽ�����ؼ�����������
����Ŀ���ұ���������������ϩ�ķ�Ӧ��![]()
��1��һ���¶��£���amol�ұ��������ΪVL���ܱ������У�����������Ӧ����Ӧʱ����������������ѹǿ���������±���
ʱ��/min | 0 | 10 | 20 | 30 | 40 |
��ѹǿ/1000kPa | 1.0 | 1.2 | 1.3 | 1.4 | 1.4 |
��ƽ��ʱ���������������ʵ����ܺ�Ϊ mol���ұ���ת����Ϊ
����ʽ������¶��¸÷�Ӧ��ƽ�ⳣ��K
��2�����ݻ�ѧ��Ӧԭ����������Сѹǿ�Ը÷�Ӧ��Ӱ��
��3��ʵ�������ķ�Ӧ�ڳ�ѹ�½��У������ұ������в���ˮ��������������ѧ���ݼ���õ��¶Ⱥ�Ͷ�ϱȶ��ұ�ת���ʵ�Ӱ�����ͼ��ʾ��[M=n��H2O��/n���ұ�]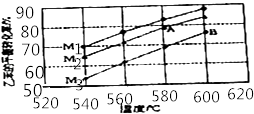
�Ƚ�ͼ��A��B�����Ӧƽ�ⳣ����С��KAKB
��ͼ��Ͷ�ϱȣ�M1��M2��M3���Ĵ�С˳��Ϊ
�����ŷ�Ӧ�Ľ��У������ϵ�������̿ʹ����Լ�����ˮ���������ڻָ������Ļ��ԣ�ԭ�������û�ѧ����ʽ��ʾ��
����Ŀ��T��ʱ����A��B��0.32mol��������ܱ������У�������Ӧ��A��g��+B��g��2C��g����H=��a kJmol��1��a��0������Ӧ�����вⶨ���������������˵����ȷ���ǣ� ��
t/min | 0 | 2 | 4 | 7 | 9 |
n��B��/mol | 0.32 | 0.24 | 0.22 | 0.20 | 0.20 |
A.����ʼʱ�������г���0.64 mol C�����ƽ��ʱ���յ�����Ϊ0.12a kJ
B.���£����ѹ�����������B��Ũ�Ⱥ��������������
C.����ʼʱ�������г��� 0.64 mol A �� 0.64 mol B�����ƽ��ʱ n��C����0.48 mol
D.���¡����ݣ���ƽ����ϵ���ٳ���0.32 mol A���ٴ�ƽ��ʱ��B��ת��������