��Ŀ����
����Ŀ����1.0molL��1KI��Һ�м������I2 �� ������Ӧ��I2��aq��+I�� ��aq���TI3����aq����H��I�������ʵ���Ũ��c��I�������¶�T�ı仯������ͼ��ʾ����֪��Ӧ��һ�δﵽƽ��ʱ��ʱ10s��������˵����ȷ���ǣ� �� 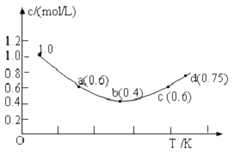
A.�÷�Ӧ�ġ�H��0
B.a��c�����Ӧ��I����Ӧ�������
C.b��ʱ0��10s I����ƽ����Ӧ����Ϊ0.04molL��1s��1
D.d��ʱ�÷�Ӧ�ڶ�Ӧ�¶��´���ƽ��״̬
���𰸡�D
���������⣺A��b������¶����ߣ���ƽ�������ƶ�����������Ӧ�Ƿ��ȷ�Ӧ�����H��0����A����
B���¶�Խ������Խ�죬c����¶ȸ���a���¶ȣ�����c������ʴ���a������ʣ���B����
C��b����ƽ��״̬��b��ʱ0��10s I����ƽ����Ӧ����Ϊv��I����= ![]() =0.060.04molL��1s��1 �� ��C����
=0.060.04molL��1s��1 �� ��C����
D��b���������ϵĵ㶼�Ƕ�Ӧ�¶��µ�ƽ��״̬������d���ڶ�Ӧ���¶��´���ƽ��״̬����D��ȷ��
��ѡD��
�����㾫�������û�ѧƽ��״̬���ʼ���������Ŀ�����жϼ��ɵõ��𰸣���Ҫ��֪��ѧƽ��״̬�����������ȡ��� V��=V��>0�����������Ƕ�̬ƽ�⣬ƽ��ʱ��Ӧ���ڽ��У�����������Ӧ������и���ְٷֺ������䣻���䡱�������ı䣬ƽ�ⱻ���ƣ������µ������½����µĻ�ѧƽ�⣻��;���أ�����������䣬���淴Ӧ�����Ǵ�����Ӧ��ʼ�����Ǵ��淴Ӧ��ʼ�����ɽ���ͬһƽ��״̬����Ч����