��Ŀ����
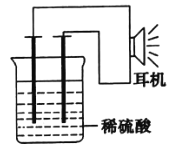
����Ŀ���������ƣ�NaH2PO2)��������ѧ�Ƽ���ʳƷ����ҵ��¯ˮ���Ӽ�����������ʵ���ҿ�����ͼ��ʾװ����ȡһ�����Ĵ������ơ���֪PH3��һ����ɫ���ж�������ȼ�����塣

�ش��������⣺
��1��װ�ռ���Һ������������___����֪NaH2PO2�����ᷴӦ��������NaOH��Һ��Ӧ��������ᣨH3PO2)��___Ԫ���ᡣ
��2��ʵ�鿪ʼʱ������Ҫ��K1��ͨ��һ��ʱ��N2����Ŀ����___��Ϊ�����ܱ���PH3��ɵĿ�����Ⱦ����жװ��ǰ��Ҫ���е�һ�������___��a�з�Ӧ�Ļ�ѧ����ʽΪ___��
��3��װ��C�����ʷ�Ӧ��������NaCl��NaH2PO2��ͨ��___�ķ����ɷ����NaH2PO2���壨��֪NaH2PO2��25��ʱ�ܽ��Ϊ100g��100��ʱ�ܽ��Ϊ667g)��
��4����Ʒ���Ȳⶨ��ȡ��Ʒmg����������ˮ���250mL��Һ������___(������ʽ��������ʽ�����ζ���ȡ25.00mL��Һ����ƿ�У�Ȼ����0.01mol��L-1��KMnO4����Һ�ζ�������������PO43-)���ﵽ�ζ��յ�ʱ����V1mLKMnO4����Һ���ζ��յ��������___����Ʒ����Ϊ___��
���𰸡���Һ©�� һ �ž�װ���еĿ�������ֹ��Ӧ���ɵ�PH3��ȼ����ը ��K1������ͨ��һ��ʱ���N2 P4+3NaOH+3H2O![]() 3NaH2PO2+PH3�� ����Ũ������ȴ�ᾧ ��ʽ ���������һ�α�Һʱ����Һ����ɫ���dz��ɫ������30s�ڲ���ɫ(��30s����ɫ���ֲ���)
3NaH2PO2+PH3�� ����Ũ������ȴ�ᾧ ��ʽ ���������һ�α�Һʱ����Һ����ɫ���dz��ɫ������30s�ڲ���ɫ(��30s����ɫ���ֲ���) ![]() %
%
��������
��1������װ��ͼ�жϣ� NaH2PO2�����ᷴӦ˵�������������ᣬNaH2PO2������NaOH��Һ��Ӧ��˵��H2PO2-���ܵ���������ӣ�
��2������PH3��һ����ɫ���ж�������ȼ�����������
��3��NaH2PO2��25��ʱ�ܽ��Ϊ100g��100��ʱ�ܽ��Ϊ667g���ܽ�����¶�Ӱ���
��4��NaH2PO2��Һ�ʼ��ԣ���������ز��ܷ�Ӧʱ�ﵽ�ζ��յ㣻KMnO4��NaH2PO2��Ӧ����Ԫ�ػ��ϼ���+7����Ϊ+2��PԪ�ػ��ϼ���+1����Ϊ+5��KMnO4��NaH2PO2��Ӧ�ı�Ϊ4:5��
��1������װ��ͼ����֪װ�ռ���Һ�������Ƿ�Һ©����NaH2PO2�����ᷴӦ˵�������������ᣬNaH2PO2������NaOH��Һ��Ӧ��˵��H2PO2-���ܵ���������ӣ����Դ����ᣨH3PO2)��һԪ���
��2��PH3����������ȼ������ʵ�鿪ʼʱ������Ҫ��K1��ͨ��һ��ʱ��N2���ž�װ���еĿ�������ֹ��Ӧ���ɵ�PH3��ȼ����ը��PH3�ж���Ϊ�����ܱ���PH3��ɵĿ�����Ⱦ����жװ��ǰ��Ҫ��K1������ͨ��һ��ʱ���N2����PH3����KMnO4��Һ���գ�a��P4���������Ƽ�������NaH2PO2��PH3�����ݵ�ʧ�����غ㣬��ƽ��Ӧ����ʽΪP4+3NaOH+3H2O![]() 3NaH2PO2+PH3��
3NaH2PO2+PH3��
��3��NaH2PO2��25��ʱ�ܽ��Ϊ100g��100��ʱ�ܽ��Ϊ667g���ܽ�����¶�Ӱ�������ͨ������Ũ������ȴ�ᾧ�ķ����ɷ����NaH2PO2���壻
��4��NaH2PO2��Һ�ʼ��ԣ��ü�ʽ�ζ�����ȡ25.00mL NaH2PO2��Һ����������ز��ܷ�Ӧʱ�ﵽ�ζ��յ㣬�����ǵ��������һ�α�Һʱ����Һ����ɫ���dz��ɫ������30s�ڲ���ɫ��KMnO4��NaH2PO2��Ӧ����Ԫ�ػ��ϼ���+7����Ϊ+2��PԪ�ػ��ϼ���+1����Ϊ+5��KMnO4��NaH2PO2��Ӧ�ı�Ϊ4:5��25.00mL NaH2PO2��Һ��NaH2PO2�����ʵ�����![]() ����Ʒ����Ϊ
����Ʒ����Ϊ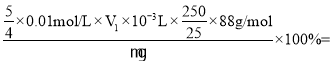
![]() %��
%��

 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�����Ŀ����ͭ����Ҫ�ɷ�ΪCu2S�����̿���Ҫ�ɷ�ΪMnO2�����Ƕ���������SiO2��Fe2O3�����ʡ���ҵ���ۺ����������ֿ����Ʊ������̺ͼ�ʽ̼��ͭ����Ҫ�����������£�
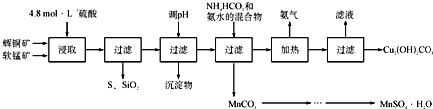
��֪����MnO2�ܽ����������е�������Ϊ������
��[Cu(NH3)4]SO4�����ȶ�������ˮ�л�ֽ�����NH3��
�����ֽ��������������������������pH��Χ���±���ʾ(��ʼ������pH����������Ũ��Ϊ1.0molL-1����)��
��ʼ������pH | ������ȫ��pH | |
Fe 3+ | 1.1 | 3.2 |
Mn2+ | 8.3 | 9.8 |
Cu2+ | 4.4 | 6.4 |
��1�����ʱ��Ϊ����߽�ȡ�ʿɲ�ȡ�Ĵ�ʩ��____________________(��дһ��)��
��2�����ڽ���ҺpH�ķ�ΧΪ____________����Ŀ����_______________________��
��3���������п�ѭ��ʹ�õ�������____________________(д��ѧʽ)��
��4���ڸù��յ����������������ڣ������ȵ��¶Ƚϵͻ���ߣ��������_________________�Ľ����
��5��̼������һ�������¿ɵ���������Һ���Ը�����������ͼʾ��������������Һ�Ʊ�MnSO4��H2O��ʵ�鷽��Ϊ____________________��
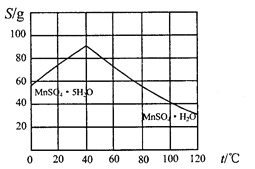
��6���ñ�BaCl2��Һ�ⶨ��Ʒ��MnSO4H2O��������ʱ��������Ʒ���ȴ���100%(�ⶨ�����в��������ɺ���)�������ԭ����_________________(��дһ��)��
����Ŀ����֪��![]() ����
����![]() ��
��![]() ��ϡ��Һ�л���ͨ�������̼����
��ϡ��Һ�л���ͨ�������̼����![]() �����Ⱥ���������ͬ�ķ�Ӧ�����ж�Ӧ��ϵ��ȷ����
�����Ⱥ���������ͬ�ķ�Ӧ�����ж�Ӧ��ϵ��ȷ����![]()
![]()
ѡ�� |
| ��Һ�����ӵ����ʵ���Ũ�� |
A. | 0 |
|
B. |
|
|
C. |
|
|
D. |
|
|
A.AB.BC.CD.D