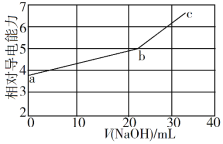
��Ŀ����
����Ŀ����þ�Ͻ��Ƿɻ����졢������������ҵ����Ҫ���ϣ��о���ѧϰС���ͬѧ��Ϊ�ⶨij��þ3%��5%����þ�Ͻ�(��������Ԫ��)��þ������������������������ֲ�ͬʵ�鷽������̽������д���пհף�
[����һ]
[ʵ�鷽��]����þ�Ͻ�������NaOH��Һ��Ӧ���ⶨʣ�����������
ʵ���з�����Ӧ�Ļ�ѧ����ʽ��___��
[ʵ�鲽��]
(1)��ȡ10.8g��þ�Ͻ��ĩ��Ʒ���������ΪV�����ʵ���Ũ��Ϊ4.0molL-1NaOH��Һ�У���ַ�Ӧ����NaOH��Һ�����V��___mL��
(2)���ˡ�ϴ�ӡ�����������塣�ò�������δϴ�ӹ��壬���þ������������___(����ƫ��������ƫ����������Ӱ����)��
[������]
[ʵ�鷽��]����þ�Ͻ�������ϡ������Һ��Ӧ���ⶨ��������������
[ʵ�鲽��]
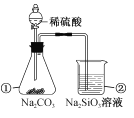
(1)ͬѧ����ѡ����ͼ1ʵ��װ�����ʵ�飺
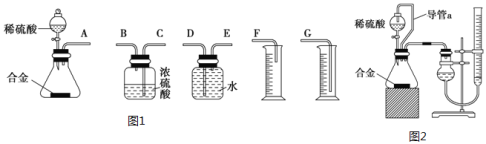
����Ϊ�����װ��������˳����A��___��___��___(��ӿ���ĸ���ɲ�����)��
(2)��ϸ����ʵ��װ�ú�ͬѧ�Ǿ�������Ϊ�������������ϴ���ϡ���������ƿ�У���ʹ������������Ҳ�Ὣƿ�ڿ����ų���ʹ�����������ƫ��ʵ�����ʱ�����ӹ��ƿ����Ͳ�ĵ�����������ˮ���ڣ�ʹ�����������ƫС�����������������ͼ2��ʾ��ʵ��װ�á�
��װ���е���a��������___��
��ʵ��ǰ���ʽ�ζ�����Һ������ֱ�ΪV1mL��V2mL����������������Ϊ___mL��
������ȷ��������������������ⶨ��������___��
���𰸡�2Al+2NaOH+2H2O=2NaAlO2+3H2�� 97 ƫ�� E D G ���ַ�Һ©��������ѹǿ����ƿ������ѹǿ��ȣ���Һ©������ʱϡ������˳�����£�������ƿ��ϡ����������ڽ����Һ©��������������Ӷ��������ڼ���ϡ������������������� V1-V2 ʵ��ʱ���¶Ⱥ�ѹǿ
��������
����һ��(1)þ������������Сʱ�������������������Ҫ������������Һ��࣬ʵ����Ҫ����������Һ�����Ӧ���ڻ�������ֵ���ݴ˼��㣻
��������(1)װ��A�кϽ���ϡ���ᷴӦ��������������������ˮ����������ˮ���ⶨ���������������ʢˮ���Լ�ƿ����һ��Ҫ�̽�����������ѹǿ��ˮ�ų���������Ͳ��ˮ������������������������Ϊ��ֹҺ��ɽ�����Ͳ�е�����Ҫ������Ͳ�ײ���
����һ����������������Һ��Ӧ����ƫ����������������Ӧ����ʽΪ2Al+2NaOH+2H2O=2NaAlO2+3H2����
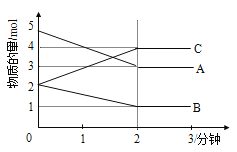
(1)��þΪ3%ʱ���������ĺ�����ߣ���ʱ���ĵ�NaOH��Һ������10.8g�Ͻ�����������Ϊ��10.8g��(1-3%)=(10.8g��97%)g��NaOH��Һ��Ũ��Ϊ4.0mol/L������ݷ���ʽ��֪�����V=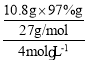 =0.097L=97mL����V(NaOH��Һ)��97mL��
=0.097L=97mL����V(NaOH��Һ)��97mL��
(2)���˵õ��Ĺ���Ϊþ��þ�ϻḽ��ƫ�����Ƶ����ʣ�δϴ�ӵ��²ⶨ��þ������ƫ��þ����������ƫ�ߣ�
��������(1)���ݷ�����֪�����װ������˳��Ϊ��(A)��(E)��(D)��(G)��
(2)��װ���е���a���Ա��ַ�Һ©��������ѹǿ����ƿ������ѹǿ��ȣ���Һ©������ʱϡ������˳�����£�������ƿ��ϡ����������ڽ����Һ©��������������Ӷ��������ڼ���ϡ������������������
�ڵζ��ܵ���̶����Ϸ������ε����֮��Ϊ�ⶨ��������������ռ�������ζ�����Һ�������С�����Բⶨ���������ΪV1-V2��
�������������¶Ⱥ�ѹǿ��Ӱ��ϴ���Ҫȷ����������ʵ���������֪��ʵ��ʱ���¶Ⱥ�ѹǿ��

 ���ɶ��ȫ���ƿؾ�ϵ�д�
���ɶ��ȫ���ƿؾ�ϵ�д�����Ŀ��ijѧ��Ϊ��̽��п�����ᷴӦ�����е����ʱ仯������100mLijŨ�ȵ�ϡ�����м���������п�ۣ�����ˮ�������ռ���Ӧ�ų���������ʵ���¼���£��ۼ�ֵ������ѻ���ɱ�״̬����
ʱ�䣨min�� | 0 | 1 | 2 | 3 | 4 | 5 |
���������mL�� | 0 | 50 | 120 | 232 | 290 | 310 |
(1)2~3min�εķ�Ӧ���ʱ�1~2min�εķ�Ӧ����__________(����������������)��ԭ����______��
(2)��2��3min����HCl��Ũ�ȱ仯����ʾ��ƽ����Ӧ���ʣ�����Һ������䣩____________��
(3)�����Ӧ̫���ң�Ϊ�˼�����Ӧ���ʶ��ֲ����ٲ������������������������зֱ����������������Һ������Ϊ���е��ǣ����ţ�____________��
A������ˮ B��NaCl��Һ C��Na2CO3��Һ D��CuSO4��Һ