题目内容
【题目】某化学兴趣小组的同学买来一瓶“84”消毒液,请大家与他们一同来研讨以下问题:
(1)此瓶“84”消毒液的说明书上这样写道:“本品为无色液体,呈碱性……”,请你推测它的有效成分( )(填序号)。
A.Cl2
B.H2O2
C.NaClO
D.KMnO4
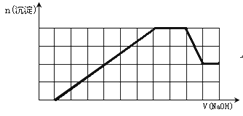
(2)该化学兴趣小组的同学在瓷碗中盛放20 mL的“84”消毒液,露置在阳光充足的室内,他们对“84”消毒液的消毒效果和组成成分的变化进行了研究。得出数据如下: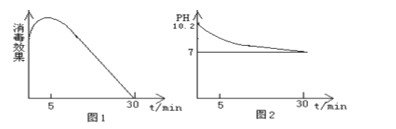
从数据图1和图2可得知“84”消毒液暴露在空气中半小时后,“84”消毒液中的主要溶质是 , 用化学方程式或离子方程式表示其中变化的主要原因
、、。
(3)该化学兴趣小组的同学选了紫色石蕊试液对“84”消毒液的性质进行实验检验,请你帮助他们完成实验报告:
实验操作 | 预期现象 | 结论 |
(4)该化学实验小组同学上网查询有关“84”消毒液的信息时,发现这样一则消息:有一家庭主妇把抗SARS用的“84”消毒液和清洁剂(呈酸性、含Cl-)都倒出一些混合在一起,进行刷洗。一会儿,她就晕倒在房间里。这几位同学感到迷惑不解。请你用离子方程式帮助他们解开这一悬念。
【答案】
(1)C
(2)氯化钠(或NaCl);2NaClO+CO2+H2O===2HClO+Na2CO3;2HClO ![]() 2HCl+O2↑;2HCl+Na2CO3===CO2↑+H2O+2NaCl(写离子方程式也可)
2HCl+O2↑;2HCl+Na2CO3===CO2↑+H2O+2NaCl(写离子方程式也可)
(3)
实验操作 | 预期现象 | 结论 |
取一干净试管,加 入1~2 mL“84” 消毒液,然后滴加 几滴紫色石蕊试液 | 先变蓝 后褪色 | “84”消毒液具有碱性和氧化性(或漂白性) |
(4)ClO-+Cl-+2H+===Cl2↑+H2O
【解析】(1)通过“本品为无色液体,”即可排除A.Cl2和D.KMnO4;通过“呈碱性……”可知为C.NaClO。(2)从数据图1和图2可得知“84”消毒液暴露在空气中半小时后,消毒效果几乎为零,溶液pH接近为7,溶液中的主要溶质应该是氯化钠(或NaCl),所发生反应的化学方程式或离子方程式表示为2NaClO+CO2+H2O===2HClO+Na2CO32HClO ![]() 2HCl+O2↑2HCl+Na2CO3===CO2↑+H2O+2NaCl(或2ClO-+CO2+H2O===2HClO+CO32-2HClO
2HCl+O2↑2HCl+Na2CO3===CO2↑+H2O+2NaCl(或2ClO-+CO2+H2O===2HClO+CO32-2HClO ![]() 2H++2Cl-+O2↑2H++CO===CO2↑+H2O)。(3)由于“84”消毒液具有碱性和氧化性(或漂白性),紫色石蕊试液遇“84”消毒液出现先变蓝后褪色的实验现象。(4)不同品牌洁污剂混合使用可能发生氯气中毒。“84”消毒液与清洁剂(呈酸性、含Cl-)混合,ClO-在酸性条件下能氧化Cl-生成氯气,发生反应的离子方程式是:ClO-+Cl-+2H+===Cl2↑+H2O。
2H++2Cl-+O2↑2H++CO===CO2↑+H2O)。(3)由于“84”消毒液具有碱性和氧化性(或漂白性),紫色石蕊试液遇“84”消毒液出现先变蓝后褪色的实验现象。(4)不同品牌洁污剂混合使用可能发生氯气中毒。“84”消毒液与清洁剂(呈酸性、含Cl-)混合,ClO-在酸性条件下能氧化Cl-生成氯气,发生反应的离子方程式是:ClO-+Cl-+2H+===Cl2↑+H2O。

 阅读快车系列答案
阅读快车系列答案【题目】锰酸锂(LiMn2O4)可作为锂离子电池的正极材料.工业上利用软锰矿浆吸收含硫烟气(SO2 和O2)制备锰酸锂,生产流程如图1: 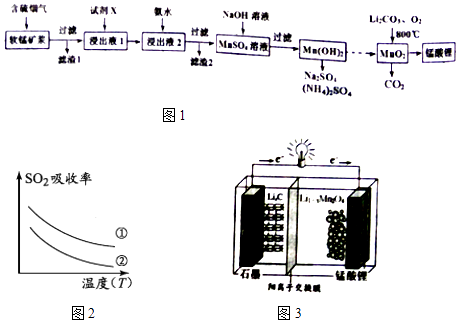
已知:①软锰矿主要成分为MnO2 , 含少量Fe2O3、FeO、Al2O3、SiO2等杂质.
②软锰矿浆在吸收含硫烟气的过程中酸性逐渐增强.
③部分氢氧化物沉淀相关的溶液pH如表一:
沉淀物 | Fe(OH)3 | Fe(OH)2 | Al(OH)3 | Mn(OH)2 |
开始沉淀 | 2.7 | 7.6 | 3.4 | 7.7 |
完全沉淀 | 3.7 | 9.6 | 4.7 | 9.8 |
(1)已知:(图2)表二 表二
实验序号 | SO2浓度(gm﹣3) | 烟气流速(mLmin﹣1) |
① | 4.1 | 55 |
② | 4.1 | 96 |
下列措施可提高SO2吸收率的是(填序号)
a.降低通入含硫烟气的温度 b.升高通入含硫烟气的温度
c.减少软锰矿浆的进入量 d.减小通入含硫烟气的流速
(2)加入试剂X能提高产品纯度,则X可以是(填化学式)
(3)加氨水调溶液pH在5~6之间,目的是 .
(4)锰酸锂可充电电池(图3)的总反应式为:Li1﹣xMnO4+LixC ![]() LiMnO4+C(x<1) ①放电时,电池的正极反应式为
LiMnO4+C(x<1) ①放电时,电池的正极反应式为
②充电时,若转移1mole﹣ , 则石墨电极将增重g.