题目内容
【题目】氮氧化物是空气的主要污染物之一,研究氮氧化物的性质对于防治空气污染有重要意义。回答下列问题:
(1)已知:NO(g)+O3(g)=NO2(g)+O2(g) △H=-200.9kJ·mol-1
NO(g)+1/2O2(g)=NO2(g) △H=-58.2kJ·mol-1
写出NO与臭氧(O3)反应生成NO2的热化学方程式______________________。
(2)温度为T1时,在三个容积均为1L的密闭容器中仅发生反应:2NO(g)+O2(g)![]() 2NO2(g) △H<0
2NO2(g) △H<0
实验测得:v正=v(NO)消耗= 2v(O2) 消耗= k正c2(NO)·c(O2),v逆=v(NO2) 消耗= k逆c2 (NO2),k正、k逆为速率常数,受温度影响。

①温度为T1时, k正/k逆=___________;当温度升高为T2时,k正、k逆分别增大m倍和n倍,则m___________n(填“>”、“<“或“=”)。
②若容器Ⅱ中达到平衡时 c(NO2)/c(NO)=1,则NO的转化率为___________,x=___________。
③容器Ⅲ中起始时v正___________v逆(填“>”、“<”或“=”),理由是___________。
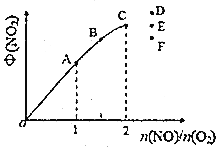
④T1时,在1L密闭容器中按照一定比例充入NO(g)和O2(g),达到平衡时NO2(g)的体积分数Φ(NO2)随n(NO)/n(O2)的变化如图所示,则A、B、C三点中NO的转化率最大的是___________;当n(NO)/n(O2)=2.3时,达到平衡时Φ(NO2)可能是D、E、F三点中的___________。
【答案】3NO(g)+O3(g)=3NO2(g) △H=-317.3kJ·mol-1 1.25 < 20% 0.85 < 因为Qc=0.22/0.32×0.25=1.78>K=1.25,反应向逆反应方向进行,所以v正<v逆 A F
【解析】
(1)根据盖斯定律求得。
(2)①根据k正/k逆=c2(NO2)/c2(NO)·c(O2)=K求出。
②根据三段式和平衡常数求算得出。
③因为Qc =0.22/0.32×0.25=1.78>K =1.25,反应向逆反应方向进行,所以v正<v逆;
④总物质的量一定时,氧气的浓度越大,NO的转化率越大,故A点最大。两者按2:1充入时,NO2的体积分数最大,当比值增大后,二氧化氮的体积分数减小。
(1)NO(g)+O3(g)=NO2(g)+O2(g) △H=-200.9kJ·mol-1①
NO(g)+1/2O2(g)=NO2(g) △H=-58.2kJ·mol-1②
2×②+①可得,3NO(g)+O3(g) = 3NO2(g) △H =-317.3kJ·mol-1,故答案为:3NO(g)+O3(g) = 3NO2(g) △H =-317.3kJ·mol-1。
(2)①根据v正=v(NO)消耗=2v(O2)消耗= k正c2(NO)·c(O2),得出k正=v(NO)消耗/c2(NO)·c(O2),
根据v逆=v(NO2)消耗= k逆c2(NO2),得出k逆= v(NO2)消耗/c2(NO2),因为v(NO)消耗= v(NO2)消耗,所以k正/k逆= c2(NO2)/ c2(NO)·c(O2)=K,
2NO(g)+O2(g)![]() 2NO2(g)
2NO2(g)
起(mol·L-1) 0.6 0.3 0
转(mol·L-1) 0.2 0.1 0.2
平(mol·L-1) 0.4 0.2 0.2
K= c2(NO2)/c2(NO)·c(O2)= 0.22/0.42×0.2=1.25,
2NO(g)+O2(g)![]() 2NO2(g) △H<0,此反应正反应是放热反应,升高温度,平衡逆向移动,平衡常数减小,由于k正/k逆=K,当温度升高为T2时,k正、k逆分别增大m倍和n倍,则m<n,故答案为:1.25;<。
2NO2(g) △H<0,此反应正反应是放热反应,升高温度,平衡逆向移动,平衡常数减小,由于k正/k逆=K,当温度升高为T2时,k正、k逆分别增大m倍和n倍,则m<n,故答案为:1.25;<。
② 2NO(g) + O2(g)![]() 2NO2(g)
2NO2(g)
起(mol·L-1) 0.5 x 0.3
转(mol·L-1) 2y y 2y
平(mol·L-1) 0.5-2y x-y 0.3+2y
达到平衡时 c(NO2)/c(NO)=1,故0.5-2y=0.3+2y,y=0.05,NO的转化率为2y/0.5×100%=2×0.05/0.5×100%=20%,K= c2 (NO2)/c2(NO)·c(O2)=0.42/0.42×(x-0.05)=1.25,x=0.85,故答案为:20%;0.85。
③容器Ⅲ中起始时v正<v逆,因为 Qc =0.22/0.32×0.25=1.78>K =1.25,反应向逆反应方向进行,所以v正<v逆;故答案为: <;因为 Qc =0.22/0.32×0.25=1.78>K=1.25,反应向逆反应方向进行,所以v正<v逆。
④总物质的量一定时,氧气的浓度越大,NO的转化率越大,故A点最大。两者按2:1充入时,NO2的体积分数最大,当比值增大后,二氧化氮的体积分数减小,当n(NO)/n(O2)=2.3时,达到平衡时Φ(NO2)可能是F点,故答案为:A;F。

 经典密卷系列答案
经典密卷系列答案 金牌课堂练系列答案
金牌课堂练系列答案 三新快车金牌周周练系列答案
三新快车金牌周周练系列答案