题目内容
【题目】硫酸工业产生的废气A(主要成分:SO2、O2、N2、CO2等)排放到空气中会污染环境。某化学兴趣小组对废气A的组成进行探究,请回答下列问题。
(1)同学甲设计实验检验废气A中含有CO2,应选择的试剂有_________。
A.NaOH溶液 B.酸性KMnO4溶液 C.澄清石灰水 D.盐酸
(2)同学乙欲测定废气A中SO2的含量,取a L废气A并设计了如下装置进行实验。
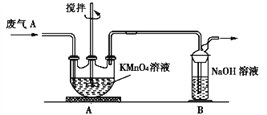
①为了保证实验成功,装置A应具有的现象是___________,搅拌的目的是___________。
②同学丙认为A装置前后的质量差就是a L废气中含有的SO2的质量,然后进行含量计算。经小组讨论后,同学丁提出疑问,按照同学丙的实验,若废气中SO2完全被吸收,则最后测定的结果应该偏大,同学丁推断的理由是_______________________________。
(3)兴趣小组的同学查阅资料发现可利用硫酸工业废气A制备皓矾(ZnSO4·7H2O)。实验模拟制备皓矾工业流程如下:
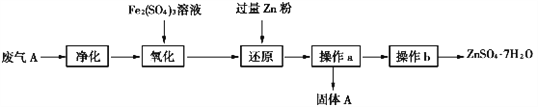
①氧化中加入硫酸铁发生反应的离子方程式是____________________。
②加入Zn粉的目的是_________________________________。
③固体A主要成分是__________________。
④操作b得到纯净皓矾晶体,必要的操作是蒸发浓缩、__________、过滤、洗涤、干燥。
【答案】 BC KMnO4溶液的紫红色不能完全褪色 提高SO2的吸收率 可能有部分SO2被O2氧化使溶液质量增加 2Fe3++ SO2+ 2H2O=2 Fe2++SO42-+4H+ 除溶液中的Fe2+、Fe3+等 Fe、Zn(或铁、锌) 结晶
【解析】试题分析:(1)硫酸工业产生的废气A(主要成分:SO2、O2、N2、CO2等)排放到空气中会污染环境,设计实验检验废气A中含有的CO2,需要除去二氧化硫,避免干扰二氧化碳的检验,除净二氧化硫的气体通过澄清石灰水检验二氧化碳的存在,石灰水变浑浊证明含有二氧化碳,所以A中为高锰酸钾溶液,B中为澄清石灰水;故答案为:BC。
(2)①为了保证实验成功需要在A装置中用高锰酸钾溶液全部吸收,高锰酸钾溶液不褪色证明二氧化硫吸收完全,搅拌的主要作用是充分吸收二氧化硫,提高吸收率;
故答案为:KMnO4溶液的紫红色不能完全褪色;提高SO2的吸收率;
②按照同学丙的实验,若废气中SO2完全被吸收,测定的结果应该偏大,可能是生成的亚硫酸被气体中氧气氧化,实验过程中发生2H2SO3+O2=2H2SO4,导致测定气体质量增大;
故答案为:2H2SO3+O2=2H2SO4;
(3)废气净化后加入硫酸铁氧化二氧化硫为硫酸,硫酸铁被还原为硫酸亚铁,加入过量锌粉还原亚铁离子和铁离子,得到固体A为锌和铁,滤液为硫酸锌溶液,通过蒸发浓缩,冷却结晶,过滤洗涤干燥等步骤得到硫酸锌晶体;
①“氧化”中加入硫酸铁发生反应是和其他中二氧化硫发生还会有反应生成硫酸亚铁和硫酸,反应的离子方程式为:2Fe3++SO2+2H2O=2Fe2++SO42-+4H+;
故答案为:2Fe3++SO2+2H2O=2Fe2++SO42-+4H+;
②加入过量锌粉还原亚铁离子和铁离子,除溶液中Fe2+、Fe3+等,故答案为:除溶液中的Fe2+、Fe3+等;
③分析可知固体A为锌和铁;故答案为:Zn、Fe;
④操作b是溶液中得到纯净皓矾晶体,必要的操作为:冷却结晶,过滤洗涤,干燥等步骤得到;
故答案为:蒸发(浓缩)、降温(结晶);