题目内容
【题目】某校化学兴趣小组同学设计实验,探究木炭与浓硫酸在加热条件下反应生成气体的成分。
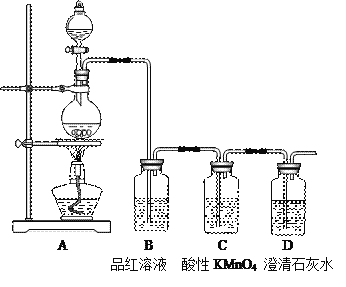
(1)写出木炭与浓硫酸反应的化学方程式____。
(2)分液漏斗使用前需检漏,方法是___。
(3)有同学对C装置能否除尽还原性气体有疑义,要确认其是否除尽,你认为对上述装置应做如何进?____。
【答案】 C+2H2SO4(浓)=CO2↑+2SO2↑+2H2O 关闭活塞,向分液漏斗中加少量水,检查旋塞芯处是否漏水,塞进玻璃塞,将漏斗倒转过来,检查玻璃塞是否漏水 在C、D之间再连接一个B装置
【解析】A中发生的反应是C+2H2SO4(浓)=CO2↑+2SO2↑+2H2O,B、确定是否含有SO2,C、除去SO2,D、检验CO2。(1)木炭与浓硫酸反应的化学方程式 C+2H2SO4(浓)=CO2↑+2SO2↑+2H2O。(2)分液漏斗使用前需检漏,方法是关闭活塞,向分液漏斗中加少量水,检查旋塞芯处是否漏水,塞进玻璃塞,将漏斗倒转过来,检查玻璃塞是否漏水。(3)要确认其是否除尽,在C、D之间再连接一个B装置。

 各地期末复习特训卷系列答案
各地期末复习特训卷系列答案 小博士期末闯关100分系列答案
小博士期末闯关100分系列答案【题目】CO、CO2是火力发电厂释放出的主要尾气,为减少对环境造成的影响,发电厂试图采用以下方法将其资源化利用,重新获得燃料或重要工业产品。

(1)CO与Cl2在催化剂的作用下合成光气(COCl2)。某温度下,向2L的密闭容器中投入一定量的CO和Cl2,在催化剂的作用下发生反应:CO(g)+Cl2(g)![]() COCl2(g)△H=a kJ/mol反应过程中测定的部分数据如下表:
COCl2(g)△H=a kJ/mol反应过程中测定的部分数据如下表:
t/min | n(CO)/mol | n(Cl2)/mol |
0 | 1.20 | 0.60 |
1 | 0.90 | |
2 | 0.80 | |
4 | 0.20 |
①反应0~2min末的平均速率v(COCl2)=_________________mol/(L·min)。
②在2min~4min间,v(Cl2)正______v(Cl2)逆 (填“>”、“=”或“<”),该温度下K=_________________。
③已知X、L可分别代表温度或压强,图1表示L一定时,CO的转化率随X的变化关系。X代表的物理量是_______________;a_______________0 (填“>”,“=”,“<”).
(2)在催化剂作用下NO和CO转化为无毒气体:
2CO(g)+2NO(g)![]() 2CO2(g)+N2(g)△H=﹣748kJ·mol﹣1
2CO2(g)+N2(g)△H=﹣748kJ·mol﹣1
①一定条件下,单位时间内不同温度下测定的氮氧化物转化率如图2所示.温度高于710K时,随温度的升高氮氧化物转化率降低的原因可能是_____________________。
②已知:测定空气中NO和CO含量常用的方法有两种,方法1:电化学气敏传感器法。其中CO传感器的工作原理如图3所示,则工作电极的反应式为___________________;方法2:氧化还原滴定法。用H2O2溶液吸收尾气,将氮氧化物转化为强酸,用酸碱中和滴定法测定强酸浓度。写出NO与H2O2溶液反应的离子方程式__________________。
(3)用CO和H2可以制备甲醇,反应为CO(g)+2H2(g)![]() CH3OH(g),以甲醇为燃料,氧气为氧化剂,KOH溶液为电解质溶液,可制成燃料电池(电极材料为惰性电极)若电解质溶液中KOH的物质的量为0.8mol,当有0.5mol甲醇参与反应时,电解质溶液中各种离子的物质的量浓度由大到小的顺序是_____________________。
CH3OH(g),以甲醇为燃料,氧气为氧化剂,KOH溶液为电解质溶液,可制成燃料电池(电极材料为惰性电极)若电解质溶液中KOH的物质的量为0.8mol,当有0.5mol甲醇参与反应时,电解质溶液中各种离子的物质的量浓度由大到小的顺序是_____________________。
选考题(19、20两题选做一题)
【题目】某课外小组设计实验室制取并提纯乙酸乙酯的方案如下:
已知:①氯化钙可与乙醇形成CaCl2·6C2H5OH
②有关有机物的沸点:
试剂 | 乙醚 | 乙醇 | 乙酸 | 乙酸乙酯 |
沸点/℃ | 34.7 | 78.5 | 118 | 77.1 |
③2CH3CH2OH![]() CH3CH2OCH2CH3+H2O
CH3CH2OCH2CH3+H2O
I.制备过程
装置如图所示,A中放有浓硫酸,B中放有9.5mL无水乙醇和6mL冰醋酸,D中放有饱和碳酸钠溶液。
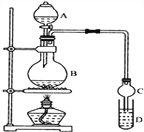
(1)写出乙酸与乙醇发生酯化反应的化学方程式______________________________。
(2)实验过程中滴加大约3mL浓硫酸,B的容积最合适的是________(填入正确选项前的字母)
A.25mL B.50mL C.250mL D.500mL
(3)球形干燥管的主要作用是_________________________。
(4)饱和Na2CO3溶液的作用是__________________________________________________________________________________________________________________________________。
II.提纯方法:①将D中混合液转入分液漏斗进行分液。
②有机层用5mL饱和食盐水洗涤,再用5mL饱和氯化钙溶液洗涤,最后用水洗涤。有机层倒入一干燥的烧瓶中,用无水硫酸镁干燥,得粗产物。
③将粗产物蒸馏,收集77.1℃的馏分,得到纯净干燥的乙酸乙酯。
(5)第①步分液时,选用的两种玻璃仪器的名称分别是__________、_______。
(6)第②步中用饱和食盐水、饱和氯化钙溶液、最后用水洗涤,分别主要洗去粗产品中的________________,__________________,______________。