题目内容
【题目】恒温恒容下,将 2 mol 气体 A 和 2 mol 气体 B 通入体积为 2L 的密闭容器中,发生如下反应:2A(g)+B(g) ![]() XC(g)+2D(s),2 min 后反应达到平衡状态,此时剩余 1.2 mol B,并测得 C 的浓度为 1.2 mol/L。
XC(g)+2D(s),2 min 后反应达到平衡状态,此时剩余 1.2 mol B,并测得 C 的浓度为 1.2 mol/L。
(1)求 X 的值__________;
(2)A 的转化率为___________;
(3)平衡前后的气体的压强之比为___________。
【答案】3 80% 1:1
【解析】
(1)2min达到平衡,C的浓度为1.2mol/L,由v=![]() =
=![]() =0.6mol/(L.min),2min时反应达到平衡状态,此时剩余1.2molB,则B的反应速率为
=0.6mol/(L.min),2min时反应达到平衡状态,此时剩余1.2molB,则B的反应速率为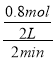 =0.2mol/(L.min),由反应速率之比等于化学计量数之比可知,X=3,故答案为3;
=0.2mol/(L.min),由反应速率之比等于化学计量数之比可知,X=3,故答案为3;
(2)2A(g)+B(g)xC(g)+2D(s),
开始 2 2 0 0
转化1.6 0.8
平衡0.4 1.2
则A的转化率之比为![]() ×100%=80%,故答案为80%;
×100%=80%,故答案为80%;
(3)恒温恒容平衡前后的气体的压强之比等于气体的物质的量和之比
2A(g)+B(g)3C(g)+2D(s),
开始 2 2 0 0
转化 1.6 0.8 2.4 1.6
平衡 0.4 1.2 2.4 1.6
则平衡前后的气体的压强之比=![]() =1:1,故答案为1:1。
=1:1,故答案为1:1。

练习册系列答案
 新思维寒假作业系列答案
新思维寒假作业系列答案
相关题目